что лучше необутин или тримедат для кишечника
Что лучше необутин или тримедат для кишечника
Е.В. Бородулина, И.В. Мареев, М.Ю. Колокольцова, И.А. Самыкина, В.В. Удут
Научно-исследовательский институт фармакологии и регенеративной медицины им. Е.Д. Гольдберга ФГБНУ «Томский национальный исследовательский медицинский центр» Российской академии наук, Томск
Введение
Синдром раздраженного кишечника (СРК) – дизрегуляторное состояние сложного генеза, при котором нарушения регуляции функциональной активности кишечника, вегетативный дисбаланс, изменения в нейрогуморальной системе, снижение выработки эндогенных опиатов реализуются с участием психосоматических наслоений. Значимую роль в становлении патологии играют нарушения кишечного микробиома и воспалительные изменения стенки кишки с цитокиновым дисбалансом. Совокупность обозначенных факторов приводит к висцеральной гиперчувствительности, нарушению моторики кишечника и замедлению транзита газов по нему, что проявляется такими симптомами, как боль, метеоризм, нарушения частоты и консистенции стула.
Принимая во внимание, что в желудочно-кишечном тракте (ЖКТ) присутствуют три основных типа опиоидных рецепторов (µ, δ и κ), а основным клиническим проявлением СРК является боль, во многом определяющаяся состоянием опиоидных рецепторов в центральных и периферических структурах, патогенетически оправдано применение при этом заболевании тримебутина, механизм действия которого заключается в стимуляции периферических энкефалиновых рецепторов, при этом связывание с κ-рецепторами приводит к снижению мышечной активности, а взаимодействие с µ- и δ-рецепторами вызывает ее активацию [1–4]. Благодаря этим эффектам тримебутин купирует дискоординацию моторики всех отделов ЖКТ, а его эффекты в отношении снижения висцеральной гиперчувствительности позитивно сказываются на проявлениях ведущего симптома СРК – боли.
Результаты значительного числа клинических исследований и богатый опыт применения препарата при нарушениях ЖКТ демонстрируют высокую эффективность тримебутина в моно- и комбинированной терапии СРК при курсе лечения от 4 до 12 недель. При этом, если и обозначаются варианты однократной дозы (от 100 до 200 мг), дискретность назначения постоянна (3 раза в сутки). То есть клинический опыт доказывает достаточность суточной дозировки в 600 мг. Вместе с тем, согласно современным данным о фармакокинетике тримебутина, а на отечественном рынке присутствуют его генерики (Необутин и Тримедат), время достижения которыми Сmax составляет 2 часа, а Т1/2 – 12 часов, повышение комплаенса без ущерба эффективности возможно реализовать двукратным приемом препарата при соблюдении суточной дозировки в 600 мг.
В соответствии с этим целью исследования стало сравнение эффективности и безопасности применения препаратов Необутин® Ретард (таблетки пролонгированного действия, покрытые пленочной оболочкой, 300 мг производства АО ФП «Оболенское», Россия) и Тримедат® (таблетки 200 мг производства ОАО «Валента Фармацевтика», Россия) больными СРК в острый период и в период ремиссии (Разрешение № 482 на проведение клинических исследований от 31.10.2012 МЗ РФ).
Материал и методы
В исследование были включены пациенты с верифицированным диагнозом «синдром раздраженного кишечника». Диагноз подтверждался наличием соответствующей клинической картины, а также результатами лабораторно-инструментального обследования. Для исключения органической патологии ЖКТ и вторичного характера функционального расстройства кишечника анализировались данные полной колоно- или сигмоидоскопии, проведенных после возникновения симптомов СРК и в течение последних 5 лет до визита рандомизации. До начала терапии клиническая картина СРК у включенных в исследование пациентов характеризовалась наличием симптомов нарушения функциональной активности ЖКТ различной степени выраженности. При первичном осмотре пациенты предъявляли жалобы на боль в животе, измененную консистенцию стула, чувство неполного опорожнения кишечника, императивные позывы на дефекацию, запоры, диарею, метеоризм.
Для равномерного распределения прогностических факторов, обеспечения надежной статистической основы оценки различий между пациентами исследуемых групп и минимизации вклада личностного фактора исследователя была предусмотрена рандомизация методом конвертов. Основная группа включала 30 человек, получавших Необутин® Ретард, таблетки пролонгированного действия, покрытые пленочной оболочкой, 300 мг (АО ФП «Оболенское», Россия) 2 раза в сутки; контрольная группа – 30 пациентов, которым назначался Тримедат®, таблетки 200 мг (ОАО «Валента Фармацевтика», Россия) 3 раза в сутки. Таким образом, суммарная суточная доза составила 600 мг для пациентов обеих групп. Исследование проведено на базе двух клинических центров. В соответствии с принципами Хельсинкской декларации на этапе скрининга получено информированное согласие пациентов. С целью верификации причин, препятствующих с медицинской точки зрения участию в исследовании, собиралась исходная информация о пациенте (демографические данные, анамнез, наследственность, перенесенные заболевания, физикальный осмотр, лабораторные данные).
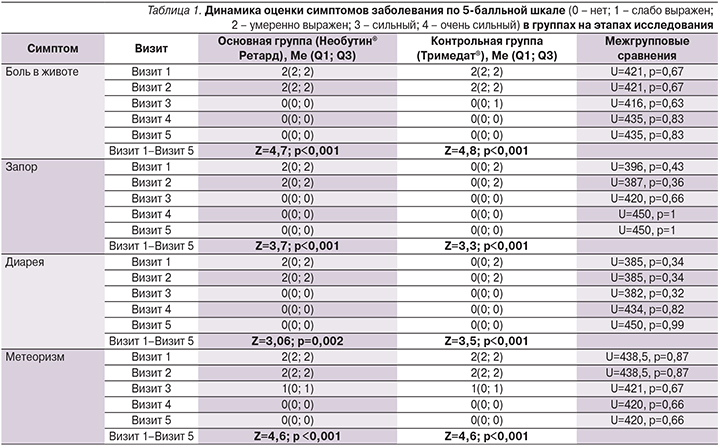
Исходно основные популяционные параметры характеризовались межгрупповой однородностью. Так, средний возраст пациентов, получавших Необутин® Ретард, составил 49±12 лет, пациентов, получавших Тримедат, – 47±11 лет, группы по данному показателю были сопоставимыми (t=0,88, p=0,38). По полу межгрупповые различия также были статистически не значимыми (χ²=0,42, p=0,519). До начала терапии интенсивность симптомов нарушения функционирования ЖКТ практически не различалась в сравниваемых группах (табл. 1).
На каждом из пяти предусмотренных протоколом визитов проведен физикальный осмотр (измерение артериального давления, частоты сердечных сокращений, температуры тела; пальпация органов брюшной полости); фиксировались и оценивались по 5-балльной шкале симптомы нарушения функционирования ЖКТ; оценивалось качество жизни по опроснику SF-36; оценивались терапия сопутствующих заболеваний, а также наличие и выраженность нежелательных явлений. Процедуры скрининга реализованы на 1-м визите. Рандомизация по группам лечения осуществлена на 1-м визите, а исследуемый препарат выдан после проведения всех требуемых по протоколу процедур на визитах 2 и 3. В отсутствие критериев невключения в исследование визит 1 (скрининг) был совмещен с визитом 2 (рандомизация). На 3-м и 4-м визитах, соответствовавших 14 и 28 дням приема препарата, также проведена оценка комплаентности лечению. Длительность терапии составила 28 дней. Заключительный визит 5 был осуществлен через 4 недели после завершения лечения.
Для обработки результатов использованы методы описательной статистики. Значения качественных показателей представлены в виде абсолютных величин, долей (N, %), в виде M±SD для количественных данных, подчиняющихся нормальному закону распределения, где M – среднее значение, SD – стандартная девиация; в виде Me (Q1; Q3) для порядковых данных и количественных данных, не подчиняющихся нормальному закону распределения, где Me – медиана, Q1 – нижний квартиль, Q3 – верхний квартиль. Сравнения количественных нормально распределенных данных произведены с использованием параметрического t-критерия Стьюдента для связанных групп. Для сравнения порядковых и количественных данных, не соответствовавших нормальному закону распределения, использованы метод знаков (Z-критерий), парный тест Вилкоксона (Wilcoxon signed-rank test). Для сравнения связанных групп данных, не подчинявшихся нормальному закону распределения, порядковых данных применен критерий Манна–Уитни (Mann-Whitney test), для бинарных качественных признаков – критерий хи-квадрат (Сhi-square test) [6].
Результаты исследования и их обсуждение
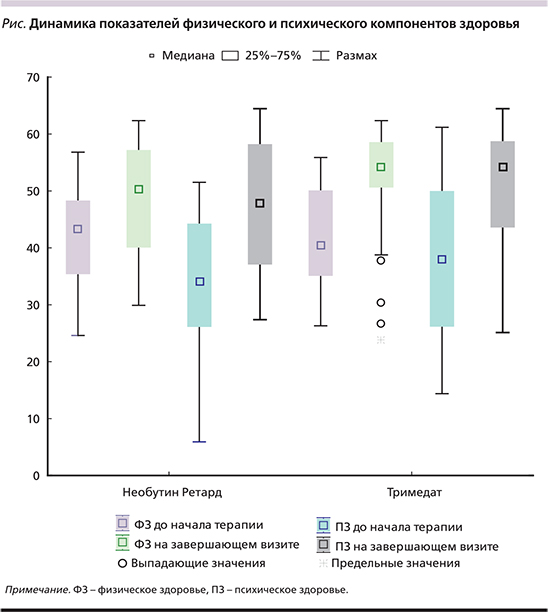
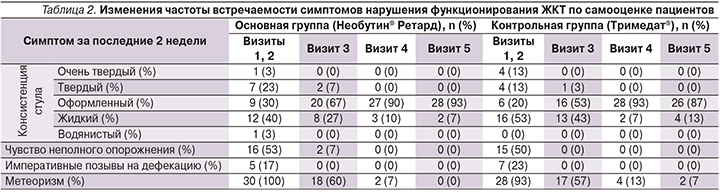
Клиническая эффективность терапии оценивалась комплексно: как по субъективным характеристикам наличия, выраженности и частоты отдельных симптомов, ощущений пациентом психического и физического компонентов здоровья, так и по клинико-лабораторным результатам динамики состояния, а также приверженности назначенному варианту терапии.
Полученные данные демонстрируют факт купирования основных симптомов СРК к окончанию срока проведения терапии: улучшение состояния отмечали все пациенты независимо от назначенного препарата (табл. 1). При этом уже через 14 дней после начала лечения проявилось значимое снижение интенсивности болевых ощущений (Z1=4,5, p
1. Белоусова Е.А. Идиопатический медленнотранзитный запор: механизмы развития и возможности лечения. Фарматека. 2010;15:18–23.
2. Нolzer P. Opioid receptors in gastrointestinal tract. Regulatory peptides. 2009;155(1–3):11–3.
3. Ивашкин В.Т., Драпкина О.М. Современные возможности применения тримебутина в лечении хронической абдоминальной боли. РЖГГК. 2008;5:12–6.
4. Тропская Н.С., Попова Т.С. Механизм действия тримебутина в коррекции функциональных расстройств желудочно-кишечного тракта. Кл. гастроэнтерология и гепатология. Русское издание. 2008;1(4):294–97.
5. Брюшинина О.С., Гурто Р.В., Соловьев М.А., Бородулина Е.В., Трифонова О.Ю., Гриднева Т.Д., Удут В.В. Проблемные вопросы изучения фармакокинетики тримебутина. Бюллетень физиологии и патологии дыхания. 2014;54:82–6.
6. Гланц С. Медико-биологическая статистика. Пер. с англ. М., 1998. С. 459.
7. Минушкин О.Н., Елизаветина Г.А. Патофизиология абдоминальной боли. Современные подходы к терапии моторных нарушений. Эффективная фармакотерапия/Гастроэнтерология. 2012;3:52–60.
8. Трухан Д.И., Гришечкина И.А., Быховцев Н.А. Тримебутин в лечении синдрома раздраженного кишечника и других функциональных гастроинтестинальных расстройств. Медицинский совет/Гастроэнтерология. 2016;19:82–6.
Тримедат: как принимать и противопоказания
Болевой синдром в области брюшной полости часто связан с нарушениями кишечной перистальтики. Спазмы мускулатуры как тонкого, так и толстого кишечника приводят к затруднению проходимости каловых масс и абдоминальной боли. Тримедат успешно снимает неприятные симптомы, нормализуя мышечный тонус кишечника.
Состав и форма выпуска
В основе синтетического средства лежит тримебутин. Он, вместе картофельным крахмалом, моногидратом лактозы и стеаратом магния образует таблетки. Дозировка предлагается фармацевтами в двух вариантах: 100 мг или 200 мг основного вещества в 1 таблетке. Внешне таблетки с разным содержанием тримебутина отличаются друг от друга: те, что содержат 100мг вещества, имеют крестообразную риску, а содержащие 200 мг – однополосную риску.
Фармакодинамика
Препарат не контролирует работу нервной системы и не воздействует на болевой центр. Его эффективность обусловлена прямым влиянием на рецепторы желудочно-кишечного тракта, расположенные по всей его длине. Снимая спазм, действующее вещество приводит перистальтику в нормальный тонус, выступает регулятором моторной функции. Не зависимо от того, какое именно заболевание вызвало спазм, тримебутин снимет боль и избавит от неприятных симптомов.
Фармакокинетика
Прием внутрь спустя полтора часа дает максимальную концентрацию тримебутина, всосавшегося из ЖКТ. Вывести препарат из крови почки и печень смогут только спустя 24 часа.
Показания к назначению
Принимают препарат для избавления или облегчения симптомов, связанных с:
спазмами кишечника при острой диарее;
синдромом раздраженного кишечника;
Кроме того, препарат эффективен в случае возникновения паралича кишечника в послеоперационный период.
Противопоказания
Лечение болей в животе Тримедатом не назначают пациентам с повышенной чувствительностью к веществам, входящим в состав таблеток. Кроме того, наличие моногидрата лактозы свидетельствует о том, что это лекарственное средство не подходит пациентам с лактазной недостаточностью.
Как принимать Тримедат
При хронических абдоминальных болях Тримедат принимают внутрь по 1 таблетке.
Частота приема для взрослых и детей, достигших 12-ти летнего возраста – трижды за день.
Детям от трех до пяти лет принимать препарат можно в дозе, равной четверти таблетки с содержанием 100мг тримебутина, то есть 1 доза=25мг.
Детям от 5 до 12 лет дают по половине таблетки, содержащей 100 мг тримебутина.
Для обеих возрастных групп прием показано осуществлять трижды в сутки.
Как долго пить Тримедат
Курс терапии зависит от симптоматики и поставленного диагноза. При эпизодической, внезапной и непродолжительной боли достаточно принимать препарат в течение суток, чтобы избавиться от симптомов. Такая ситуация характерна при нетоксичных пищевых отравлениях, когда с очищением кишечника прекращаются и неприятные симптомы. Тримедат в этом случае снимет спазмы и нормализует резкие сокращения кишечника, приводящие к болям.
В случае диагностирования синдрома раздраженного кишечника назначают двухнедельную терапию. После исчезновения неприятных симптомов терапию не прекращают. Для сохранения положительного эффекта, с целью исключить рецидив Тримедат продолжают принимать в течение еще 3 месяцев.
Как принимать Тримедат при запорах
Причины запора и его характер определяет продолжительность приема медикаментов. В случае разовой задержки стула, обусловленного неправильным питанием и малой подвижностью, достаточно принимать препарат трижды в день в стандартной дозировке до тех пор, пока кишечник не сможет опорожниться. Чаще всего на это уходят сутки, реже – до5 дней. Отсутствие рецидива в этом случае может гарантироваться сам пациент, изменив пищевые привычки и наладив ежедневную двигательную активность.
В случае запоров, возникших на фоне кишечной непроходимости, обусловленной нарушением кровообращения в нижней полой вене, Тримедат принимают длительным курсом, начиная от 4 недель. Для исключения рецидива и усугубления ситуации больному показана диета, с высоким содержанием продуктов растительного происхождения, богатых клетчаткой. Такой подход к питанию обеспечит мягкость стула, что существенно облегчит его прохождение по кишечнику, и исключит случаи травмирования стенок твердыми комочками кала.
Как принимать Тримедат: до или после еды
Работать препарат начинает спустя час после попадания в желудочно-кишечный тракт. Для того чтобы прием пищи не стал причиной появления болей, отрыжки, вздутия и других неприятных симптомов, выпивать Тримедат следует за 20-30 минут до предполагаемого приема пищи. Когда еда будет обработана желудочным соком и попадет в двенадцатиперстную кишку, препарат уже начнет действовать и не позволит пище застояться, что снизит риск развития процессов гниения, которые и вызывают метеоризм, тошноту и отрыжку.
Что лучше: Тримедат или Необутин
Оба препарата созданы на основе тримебутина. Необутин не может стать препаратом выбора для больных с лактазной недостаточностью, так как вспомогательные компоненты Необутина такие же, как у Тримедата, включающие моногидрат лактозы. Препараты абсолютно идентичны.
Что дешевле: Тримедат или Необутин
Средняя цена на Тримедат, включающий 200мг активного вещества в 1 таблетке, 30 штук в упаковке – 650 рублей. А средняя стоимость Необутина в той же дозировке действующего вещества, за упаковку из 30 таблеток – 470 рублей.
Что лучше: Дюспаталин или Тримедат
Дюспаталин, в отличие от Тримедата, основан на действии мебеверина. В составе капсул нет лактозы, поэтому этот препарат может быть использован в качестве медикамента, снимающего боль в кишечнике, даже у пациентов с непереносимостью лактозы. Спазмолитический эффект при длительной терапии сохраняется при приеме препарата дважды в сутки, что удобнее, чем три приема для Тримедата.
Что лучше необутин или тримедат для кишечника
Функциональные гастроинтестинальные расстройства (ФГИР) в настоящее время рассматриваются как наиболее распространенная патология желудочно-кишечного тракта (ЖКТ), в основе которой лежат комбинированные морфологические и физиологические отклонения, связанные с висцеральной гиперчувствительностью, нарушениями моторики ЖКТ, защитного слизистого барьера, иммунной функции и состава кишечной микробиоты, а также расстройствами со стороны центральной нервной системы (ЦНС).
Изучением патофизиологии ФГИР, разработкой, совершенствованием и внедрением их классификации, диагностических критериев и практических алгоритмов ведения пациентов занимается международная группа экспертов. В мае 2016 года состоялась официальная презентация «Римских критериев- IV», которые определяют ФГИР как «расстройства взаимодействия «кишка–головной мозг» («ЖКТ-ЦНС») (disorders of gut-brain interaction) [1].
В последней редакции «Римских критериев» официальное признание получил синдром перекреста функциональных нарушений (overlap syndrome), т.е. возможность наличия у пациента одновременно нескольких функциональных нарушений и переход их из одной формы в другую, например сочетание СРК и ФД [1].
Практикующему врачу, с учетом многообразия клинической картины функциональных нарушений, приходится часто корректировать лечение в связи с меняющейся клинической картиной, в том числе при сочетанных функциональных нарушениях, например СРК+ФД, СРК + билиарная дисфункция, ФД + билиарная дисфункция, а также при смене клинического варианта СРК. Все это требует пересмотра подхода к терапии и заставляет врача постоянно изменять тактику лечения.
Соответственно актуальным является оптимизация лекарственной терапии, подразумевающая в лечебной тактике ФГИР приоритет применения препаратов, обладающих мультитаргетным эффектом, влияющим одновременно на несколько патогенетических звеньев этих заболеваний или же оказывающим благоприятное действие при наличии коморбидной патологии. К патогенетическим факторам ФГИР, которые можно считать доказанными в настоящее время, относятся нарушения моторики ЖКТ и висцеральная гиперчувствительность [2, 3].
Одним из широко применяемых и хорошо изученных регуляторов моторики является тримебутин – универсальный регулятор моторики ЖКТ, который является полным агонистом всех трех типов периферических опиоидных рецепторов. Тримебутин – 2–(диметиламино)–2–фенилбутилэфир 3,4,5–триметоксибензойной кислоты – синтезирован Laboratoires Jouveinal (Франция) в 1969 г. По фармакологическому указателю тримебутин относится к группам «Спазмолитики миотропные» и «Стимуляторы моторики ЖКТ, в том числе рвотные средства». По АТХ – к группе «Препараты для лечения функциональных расстройств кишечника» и имеет код A03AA05.
Механизм действия тримебутина заключается в стимуляции периферических опиоидных (энкефалиновых) рецепторов (μ-, k-, δ-) на протяжении всего желудочно-кишечного тракта (ЖКТ). Связывание с k-рецепторами приводит к снижению мышечной активности, а связывание с μ- и δ-рецепторами вызывает ее стимуляцию. При этом препарат не оказывает влияние на другие рецепторы. Тримебутин оказывает прямое действие на гладкомышечные клетки через рецепторы на миоцитах и в ганглиях энтеральной нервной системы, имитируя действие энкефалинов [4, 5]. Описано воздействие Тримебутина на Na+ каналы, обуславливающие анестезирующее действие препарата и прямой спазмолитический эффект [6]. Тримебутин воздействует на антиноцицептивную систему организма с повышением порога болевой чувствительности, модификацией оценки боли, снижением чувствительности рецепторов к медиаторам воспаления. Более того, тримебутин обладает местным обезболивающим действием, которое в 17 раз превышает действие лидокаина [7]. Отмечено и влияние тримебутина на потенциал-зависимые Ca каналы: L-тип Ca++ каналов / BKca каналы, что объясняет его физиологичность: тримебутин поддерживает гомеостаз мышечной клетки в ЖКТ, за счет того, что ограничивает выход К+ из клетки [8].
Тримебутин стимулирует эвакуаторную функцию желудка, нормализует моторику кишечника, способствует купированию ощущения вздутия и дискомфорта, благоприятно действует как при гиперкинетических, так и при гипокинетических формах нарушений моторной деятельности ЖКТ [7, 8]. Действие тримебутина на висцеральные сенсорные афферентные нервы дополняет его благоприятный эффект при лечении функциональных заболеваний ЖКТ. Кроме того, тримебутин оказывает влияние и на гуморальную регуляцию моторики ЖКТ, активируя энтеральную нервную систему, способствуя высвобождению желудочно-кишечных гормонов – мотилина, вазоактивного интестинального пептида (ВИП), гастрина и глюкагона, обладающих прокинетическим потенциалом [4, 9, 10].
Таким образом, тримебутин является селективным желудочно-кишечным спазмолитиком с выраженной анастезирующей и прокинетической активностью. На протяжении многих лет тримебутин применяется в различных странах мира для лечения функциональных нарушений ЖКТ у взрослых и детей.
Эффективность тримебутина при лечении синдрома раздраженного кишечника (СРК) продемонстрирована в ряде мета-анализов [11–14] и обзоров [9, 15]. Тримебутин благоприятно действует как при гипокинетических, так и при гиперкинетических формах нарушений моторной деятельности кишечника. Тримебутин назначают по 100 – 200 мг 3 раза в сутки, перед едой (на курс 3–4 недели). У больных с СРК с преобладанием кишечной гипотонии исключительно эффективен тримебутин по 300 мг/сут, через 7 дней дозу увеличивают до 600 мг/сут. [9]. Модулирующий эффект тримебутина на моторику кишечника у больных СРК продемонстрирован в российском исследовании [10], в котором через 4 недели терапии препаратом тримебутином в суточной дозе 600 мг у пациентов с СРК с запорами частота стула увеличилась у 94 % больных, а у пациентов с СРК с диареей уменьшилась у 75 % больных. В рандомизированном исследовании, проведенном в Китае, включавшем пациентов с функциональной диспепсией и СРК с диареей, показана высокая эффективность тримебутина в коррекции диареи [16].
При проведении клинических исследований разные авторы относили тримебутин к различным фармакологическим группам, в зависимости от механизма влияния на ЖКТ. При изучении действия тримебутина на гиперкинетические расстройства моторики и выраженность абдоминальной боли исследователи относили препарат к группе спазмолитиков [12], а при изучении его влияния при гипокинетических расстройствах ЖКТ препарат расценивался как прокинетик [17]. Ретроспективное наблюдение в течение 4 лет за пациентами с СРК свидетельствует о наибольшей эффективности в лечении СРК тримебутина в комбинации с анксиолитиками и пробиотиками [18]. Эффективность тримебутина в лечении пациентов с хроническим запором: увеличение толстокишечного транзита и частоты стула – отмечена и в ряде других исследований [19–21].
В сравнительных исследованиях отмечена сравнимая клиническая эффективность тримебутина с другими спазмолитиками: пинаверия бромидом [22], мебеверином [23, 24] и феноверином [25] в лечении пациентов с СРК.
Тримебутин представляется препаратом выбора при сочетанной патологии – ФД и СРК как наиболее частой ассоциации нарушений моторики (желудок, двенадцатиперстная кишка, кишечник). Эффект тримебутина связан с восстановлением разных форм расстройств моторики желудочно-кишечного тракта (как верхних – желудок, двенадцатиперстная кишка, так и толстого кишечника) [26–29]. Ускорение опорожнения желудка в сочетании со снижением висцеральной гиперчувствительности позволяет тримебутину эффективно воздействовать и на симптомы ГЭРБ, что было продемонстрировано в греческом исследовании при лечении тримебутином пациентов с СРК и сопутствующей ГЭРБ [30]. В исследовании прокинетических эффектов тримебутина было показано ускорение эвакуации жидкости из желудка на 19 % и модулирующее действие тримебутина на электрическую активность ЖКТ [31].
В одном из первых исследований применения тримебутина при патологии билиарного тракта была отмечена его эффективность регуляции моторики и тонуса сфинктера Одди после холецистэктомии [32]. Дальнейшее исследование применения тримебутина в терапии пациентов с функциональными расстройствами билиарной системы подтвердило, что тримебутин эффективно купирует симптомы функциональных и диспепсических расстройств у большинства пациентов с дисфункциями желчного пузыря и сфинктера Одди [4, 33]. Четырехнедельный курс терапии тримебутином 200 мг 3 раза в день приводит к нормализации сократительной функции желчного пузыря у больных с функциональными расстройствами как гипомоторного, так и гипермоторного типа. Тримебутин оказывает спазмолитическое действие на сфинктер Одди у больных желчнокаменной болезнью, перенесших холецистэтомию, что подтверждается существенным уменьшением диаметра холедоха к завершению курсовой терапии у большинства пациентов. При этом тримебутин хорошо переносится больными, не оказывает побочных эффектов и не влияет на показатели клинического и биохимического анализа крови, что подтверждает его безопасность [4]. Исследование на здоровых пациентах показало отсутствие влияния на ЧСС и показатели автономной нервной системы [34].
Еще одним свидетельством безопасности тримебутина является и опыт его применения в педиатрической практике. Тримебутин в форме суспензии разрешен к применению с младенческого возраста, в таблетированной форме с 3-летнего возраста.
Согласно многочисленным обзорам [35, 36], применение тримебутина у детей с СРК высокоэффективно (имеет уровень доказательности В) и безопасно. В исследовании C. Dupont и соавт. [8] был показан достоверный положительный эффект применения тримебутина у детей с функциональными нарушениями моторики желудочно-кишечного тракта. В турецком исследовании [37] у 345 детей (4–18 лет) с СРК терапия тримебутином была эффективна у 94,9 % группы тримебутина по сравнению с 20,5 % группы сравнения, в которой использовались немедикаментозные методы (р