что лучше омник окас или тамсулозин вертекс
Сравнительный анализ препаратов Кардура, Омник и Урорек
Каждый из рассматриваемых мною препаратов изложен в Интернете на сайтах, специально посвященных лекарствам от простатита, поэтому я не буду уделять подробного внимания ни механизму действия, ни формам выпуска, ни фармакокинетике и фармакодинамике, ни другим сложным и интересным лишь для профессионала характеристикам. Считаю важным рассматривать средства от простатита лишь с точки зрения врача уролога с опытом работы 15 лет.
На всякий случай уточняю. Я не сотрудничаю ни с какой фармфирмой и не занимаюсь ни рекламой, ни антирекламой препаратов, а так же не претендую на истину в последней инстанции. Это всего лишь мое мнение, написанное исключительно для моих пациентов.
Все три препарата относятся к классу так называемых адреноблокаторов. Точкой приложения этой группы являются адренорецепторы, отвечающие за расслабление гладкой мускулатуры. Поскольку гладкие мышцы образуют стенку органов ЖКТ, мочевой системы и сосудов первый препарат этой группы «Кардура» фирмы «Пфайзер» помимо основного, положительного, эффекта (о нем поговорим чуть ниже) вызывает два нежелательных эффекты – снижение моторики кишечника и снижение АД (вплоть до его резкого падения — коллапса). Для того, чтобы минимизировать эти нежелательные эффекты фирма производитель рекомендует работать с дозой препарата (постепенно наращивают, подбирая необходимую). Это сложно и долго и для пациента и для врача. Поэтому, по моему мнению, «Кардура» имеет право на жизнь только при аллергии на все другие альфаблокаторы.
Главный положительный эффект препаратов данной группы является быстрое и выраженное уменьшение таких нарушений мочеиспускания, как затрудненное мочеиспускание и неполное опорожнение мочевого пузыря. Т.е. мы можем рассчитывать ТОЛЬКО на быстрый локальный тактический результат (симптоматическое лечение). Ни о каком полноценном лечении простатита или аденомы не может быть и речи.
В чем разница этих двух препаратов. Окас можно разжевывать до порошка – это никак не влияет на его работу. А вот с Омником такого делать категорически нельзя. Поэтому Окас хорошо идет пациентам, у которых есть затруднения при глотании таблеток (пожилые, люди после операций на пищеводе и др.).
Урорек позиционируется фирмой «Рекодати» как еще более селективный препарат (еще меньше % побочных эффектов). Однако на практике я не заметил у него принципиальных отличий от Омника. В то же время купить его в аптечной сети гораздо труднее.
Важный нюанс. И Омник, и Урорек – это мощные, хорошие, достаточно эффективные препараты, с относительно низкой частотой побочных эффектов, но – только если правильно рассчитана доза, время и длительность приема с учетом ряда параметров. Стандартная, наиболее распространенная схема, такова — 1 таб. 1 раз в день, утром, 7-30 дней. Однако, следует помнить, что отсутствие коррекции препараты с учетом работы ССС, веса и аллергического анамнеза может привести к тому, что возникнут серьезные побочные эффекты или препараты дадут очень слабый эффект.
И последнее. Некоторые пациенты могут мне возразить: «Доктор, а вот я (или мой хороший знакомый) вот уже год или два пьем только Омник Окас и чувствуем себя хорошо». Да, некоторые симптомы нижних мочевых путей Омник действительно снимает очень хорошо (и еще поэтому я достаточно часто использую альфаблокаторы), но на основной процесс воспаления он НЕ ДЕЙСТВУЕТ. По данным обследования у таких пациентов простатит исподволь прогрессирует (в этом коварство простатита) и через некоторое время Омник, а вместе с ним ряд других лекарств, просто перестает действовать – развиваются осложнения в виде падения потенции, увеличивается риск аденомы простаты и т. д.
Резюмируя вышесказанное хочу сказать, что если у пациента по тем или иным причинам нет возможности посетить уролога в ближайшее время, а нарушения мочеиспускания резко ухудшают его качество жизни прием Омника, Омника Окаса или Урорека на короткое время вполне оправдан.
После написания этой статьи я получил от пациентов ряд писем, одно из которых хочу опубликовать.
«Дмитрий Анатольевич, принимал Кардуру. Полностью согласен с вышеописанным. Давление падало, с кишечником было не очень, да еще на фоне дисбактериоза кишечника. Но от кардуры не было ретроградной эякуляции. Пропил курс Кардуры месяц. Сейчас врач назначил мне Урорек, хотя я просил не назначать препараты с ретроградной эякуляцией. В свое время врач мне из-за этого отменял омник. Но видимо уже не помнит, назначил похоже другую марку, вместо омника и все. Другой уролог мне предлагает пропить дальфаз ретард, Который стоит в 2-3 раза дороже, почти 2 000 рублей. Говорит, что эффект от него хороший, а побочных эффектов с эякуляцией нет, или менее выражены. Подскажите, пожалуйста, как ведет себя Дальфаз ретард в сравнении с Урореком, Кардурой? Может быть есть вообще какая-то растительная замена этим всем блокаторам? Сейчас я еще принимаю Гентос. Еще раз спасибо за статью.»
Ответ: Здравствуйте. Дальфаз, на мой взгляд, принципиально не отличается от других препаратов этой группы. Его «великолепное действие» на практике обычно. В тоже время за бренд переплата достаточно высокая.
Гиперплазия простаты: скальпель или таблетки?
Современная медикаментозная терапия доброкачественной гиперплазии простаты
Л.М.Гориловский, д.м.н., профессор, Д.А.Лахно, к.м.н., НИИ урологии, Москва
Журнал «Медицинский совет» № 7-8 (2010)
Опубликовано на сайте «Ремедиум»
Одним из наиболее распространенных урологических заболеваний мужчин пожилого возраста является доброкачественная гиперплазия предстательной железы (ДГП). По эпидемиологическим данным, распространенность ДГП в большинстве стран достигает 20% у 50-летних мужчин, 50% – у 60-летних, 57% – у 70-летних и 80% – у 80-летних. Средняя обращаемость по поводу ДГП в России, по данным Н.А.Лопаткина и соавт., в 2000 г. составила 113–125 на 100 000 мужского населения. Вероятность подвергнуться оперативному лечению у мужчины в возрасте от 60 лет с гиперплазией простаты и симптомами нижних мочевых путей (СНМП), согласно данным некоторых исследователей, достигает 39% [1].
Таким образом, ДГП является одним из самых распространенных заболеваний, приводящих к оперативному вмешательству. Возрастающая продолжительность жизни ведет к увеличению числа мужчин, страдающих ДГП, а улучшение качества их жизни понижает толерантность к заболеванию, не позволяя продолжать активный образ жизни.
Демографические исследования Всемирной организации здравоохранения, свидетельствующие о значительном росте населения в возрасте старше 60 лет, подчеркивают социально-экономическую значимость и актуальность данной проблемы. Темпы роста данного заболевания существенно опережают рост населения планеты в целом. Следует отметить, что пожилое население обладает большим жизненным, производственным и интеллектуальным потенциалом, который должен в полной мере использоваться обществом.
Прогрессирование ДГП заключается в ухудшении клинических показателей, включая увеличение объема предстательной железы, утяжеление СНМП и снижение максимальной объемной скорости мочеиспускания (Qmax), повышение риска развития острой задержки мочеиспускания (ОЗМ) и возникновение необходимости в оперативном лечении ДГП, а также снижении качества жизни, связанном с ДГП [2].
В связи с тем, что учащенное мочеиспускание, вялая струя мочи, странгурия, ночная поллакиурия, являющиеся основными симптомами ДГП, значительно ухудшают качество жизни, основная задача уролога заключается в своевременной диагностике этих заболеваний и проведении ранних лечебных мероприятий, направленных на повышение качества жизни (Гориловский Л.М., 2004).
Согласно современным представлениям диагностический комплекс при обследовании больного ДГП включает: сбор анамнеза, количественную оценку симптомов и «качества жизни» с помощью Международной шкалы оценки симптомов заболеваний простаты – IPSS (таблица приведена в статье «Аденома простаты: знай свой маневр» – ВМ); исследование уровня простатического специфического антигена (ПСА), мочевины и креатинина сыворотки крови; анализ мочи и секрета простаты; пальцевое ректальное исследование; трансабдоминальное ультразвуковое исследование почек и мочевого пузыря с определением количества мочи; трансректальную ультрасонографию, урофлоуметрию. В некоторых случаях необходимо выполнение уродинамических исследований.
Еще до недавнего времени уролог и пациент с диагнозом ДГП стояли перед выбором: либо проводить оперативное лечение, либо ждать и наблюдать. Под оперативным лечением подразумевались чреспузырная или позадилонная простатэктомия или трансуретральная резекция простаты с ее модификациями. В последнее время, наряду с увеличением частоты заболеваемости ДГП, значительно увеличилось количество методов лечения этих больных. Прежде всего появились лекарственные препараты, с помощью которых можно добиться хорошего эффекта, особенно на начальных стадиях заболевания.
Успехи в познании патогенеза гиперплазии предстательной железы и создании медикаментозных препаратов с патогенетически направленным механизмом действия привели к тому, что лекарственная терапия определенных категорий больных стала по-настоящему эффективной. Современная фармакотерапия позволяет многим пациентам избежать нежелательного оперативного лечения и связанных с ним грозных осложнений, таких как необратимое недержание мочи и потеря сексуальной функции с последующим нарушением качества жизни [3].
И хотя медикаментозное лечение не избавляет пациента от гиперплазии предстательной железы, оно дает возможность значительно уменьшить жалобы, улучшить нарушенное мочеиспускание и нормализовать качество жизни. Лекарственная терапия при симптомах нижних мочевых путей активно применяется в течение 15 лет при ДГП. В начале 1990-х годов появились селективные α-адреноблокаторы длительного действия – теразозин и доксазозин, а несколькими годами позже на фармацевтическом рынке появились первые ингибиторы 5α-редуктазы. Эти две группы препаратов стали основными для лечения ДГП, резко сократив количество трансуретральных резекций простаты. Например, в США число трансуретральных и открытых аденомэктомий уменьшилось с 250 000 в 1987 г. до 88 000 в 2000 г. [4].
При выборе метода лечения врач должен оценить данные инструментальных методов исследования и имеющиеся у пациента проблемы, отраженные в опроснике IPSS. В качестве элемента стандартного обследования подобных больных рекомендуется оценить субъективное восприятие тяжести симптомов ДГПЖ и эффективности его лечения. Это связано с тем, что наиболее частые симптомы нередко не являются наиболее беспокоящими больных [5].
Диагностическими критериями для назначения консервативной терапии при постановке диагноза ДГП служат: суммарный балл IPSS больше 7 и меньше 19; максимальная скорость потока мочи (Qmax) более 5 мл/с; объем остаточной мочи не более 150 мл; наличие противопоказаний к оперативному лечению в связи с сопутствующими заболеваниями; отказ пациента от операции. Согласно 4-й Международной консультации по ДГП (1997) абсолютными показаниями к оперативному лечению являются: задержка мочи; рецидивирующая макрогематурия, обусловленная доброкачественным увеличением предстательной железы; большие дивертикулы мочевого пузыря; почечная недостаточность, камни мочевого пузыря или рецидивирующие инфекции мочеполового тракта, обусловленные инфравезикальной обструкцией [6].
Группой выбора для симптоматического лечения обструктивных симптомов ДГП являются блокаторы α-адренергических рецепторов, воздействие которых направлено на элементы автономной нервной системы, которые являются составляющими в динамическом компоненте инфравезикальной обструкции при ДГП. Альфа-адреноблокаторы уменьшают симптоматику и улучшают уродинамические показатели, однако в настоящее время не продемонстрировано подобное их воздействие в отношении остановки прогрессии ДГП и уменьшения риска необходимости хирургического лечения ДГП.
Тамсулозин (омник (Astellas Pharma); тулозин (Egis)) – наиболее действенный α-адреноблокатор, использующийся для медикаментозного лечения ДГП. Его уникальные особенности применения (эффективность без побочных воздействий, отсутствие необходимости в титровании дозы, отсутствие влияния на артериальное давление) могут быть обусловлены как относительно низкой терапевтической дозировкой в 0,4 мг при наибольшем α-блокирующем воздействии, так и селективностью к подтипу (α1а-адренорецепторов). Тамсулозин избирательно и конкурентно блокирует постсинаптические α1А-адренорецепторы, находящиеся в гладкой мускулатуре предстательной железы, шейки мочевого пузыря и простатической части уретры. Это приводит к снижению тонуса гладкой мускулатуры предстательной железы, шейки мочевого пузыря и простатической части уретры, улучшая отток мочи. Одновременно уменьшаются симптомы обструкции и раздражения, связанные с доброкачественной гиперплазией предстательной железы.
Способность тамсулозина воздействовать на α1А-адренорецепторы в 20 раз превосходит его способность взаимодействовать с α1В-адренорецепторами, расположенными в гладких мышцах сосудов. Благодаря высокой селективности препарат не вызывает какого-либо клинически значимого снижения системного АД как у пациентов с гипертензией, так и у пациентов с нормальным исходным АД. Биодоступность тамсулозина составляет около 90%, а стабильная концентрация в крови при ежедневном приеме достигается в среднем за 5 дней. Основным местом метаболизма тамсулозина является печень, а важную роль в этом процессе играют ферменты из группы цитохромов. Наиболее часто встречающимися побочными эффектами тамсулозина являются заложенность носа, головные боли и нарушение эякуляции. Большое клиническое значение имеют фармакологические характеристики тамсулозина. Отсутствие значимого действия на сердечно–сосудистую систему позволяет избежать титрования дозы тамсулозина. Таким образом достаточно быстро достигается максимальный клинический эффект от его применения. Клиническая эффективность тамсулозина в стандартной дозе (0,4 мг 1 раз в сутки) была тщательно изучена в нескольких многоцентровых рандомизированных, плацебо–контролируемых, двойных слепых исследованиях, проведенных в Европе и Северной Америке, в которых приняли участие более 1300 пациентов. Эти исследования подтвердили долгосрочный характер эффективности и безопасности тамсулозина в качестве препарата для фармакотерапии доброкачественной гиперплазии предстательной железы [7].
Омник окас представляет собой таблетку с контролируемым высвобождением на основе матрикса с использованием геля неионного типа, что обеспечивает длительное и медленное высвобождение тамсулозина и дает достаточную экспозицию со слабыми колебаниями в течение 24 ч. Благодаря этому обеспечивается круглосуточный эффективный контроль над симптомами нижних мочевых путей.
Данные нескольких международных исследований эффективности применения α-адреноблокаторов свидетельствуют, что многие пациенты, наряду с уменьшением выраженности СНМП, отмечают улучшение половой функции. Предполагают, что причиной подобного эффекта является поливалентный механизм действия α-адреноблокаторов, способствующий улучшению кровообращения органов малого таза и общему повышению качества жизни больного [8].
Как было отмечено выше, при всех своих достоинствах α-адреноблокаторы не способны влиять на прогрессию заболевания. В случае высокого риска прогрессии заболевания (объем предстательной железы превышает 50–60 см3) рекомендовано вводить в терапию ингибиторы 5α-редуктазы. Известно, что ингибиторы 5α-редуктазы способны тормозить прогрессирование заболевания в результате угнетения превращения тестостерона в дигидротестостерон, андроген, который считают основным фактором, влияющим на гиперпластический рост ткани предстательной железы. Ингибиторы 5α-редуктазы не только тормозят дальнейший рост ДГП, но и уменьшают размеры простаты, если она увеличена [9,10]. Из числа применяемых для консервативного лечения мужчин, страдающих ДГП, препаратов лишь ингибиторы 5α-редуктазы способны влиять на патофизиологические механизмы, лежащие в основе заболевания. Существует две изоформы 5α-редуктазы (тип 1 и тип 2). Сегодня в России доступны два препарата из группы ингибиторов 5α-редуктазы, достоверно уменьшающих объем предстательной железы – финастерид и дутастерид. Финастерид, который блокирует 5α-редуктазу 2 типа, известен уже давно, и эффект от его назначения становится очевиден, в среднем, через полгода лечения. Дутастерид является в 45 раз более мощным ингибитором 5α-Р 1 типа, чем финастерид, и в 2,5 раза более мощным ингибитором 5α-Р 2 типа. Он обеспечивает более выраженную супрессию ДГТ в сыворотке (α93% против 70%). Эти характеристики обусловливают более раннее наступление эффекта: уменьшение размера простаты и увеличение Qmax. В западных странах дутастерид под коммерческим названием аводарт был зарегистрирован и разрешен для клинического использования в 2002 г., в России – в 2005 г. Эффективность и безопасность дутастерида была оценена в обобщенном анализе, включавшем 3 плацебо-контролируемых, двухлетних, дважды слепых исследования.
Уже через 2 недели после начала лечения дутастеридом происходило снижение уровня дигидротестостерона сыворотки более чем на 90%, причем это снижение сохранялось до конца исследования. За 2 года объем простаты снизился на 25,7%. Кроме этого, на фоне лечения дутастеридом отмечено стойкое снижение выраженности симптомов заболевания, увеличение Qmax и снижение риска развития ОЗМ на 57% и возникновение необходимости в оперативном лечении на 48% [11]. Для взрослых мужчин, включая пациентов пожилого возраста, рекомендуемая доза при приеме внутрь составляет 500 мкг (1 капс) 1 раз в сут.
Наиболее значимыми побочными эффектами при монотерапии дутастеридом являются: импотенция, изменение (снижение) либидо, нарушение эякуляции, гинекомастия. Анализ данных, полученных в ходе упомянутых выше плацебо-контролируемых исследований, показал, что имевшие место нежелательные явления, как правило, были слабой или умеренной степени выраженности и чаще всего относились к расстройствам сексуальной функции. При этом как в группе приема аводарта, так и в плацебо-группе у подавляющего большинства пациентов (соответственно, у 89 и 94%) расстройств сексуальной функции не было. Следует отметить, что по частоте регистрируемых нежелательных явлений, связанных с приемом препаратов, статистически достоверные отличия между группами дутастерида и плацебо, как правило, наблюдались только в течение первых 6 месяцев терапии. В ходе дальнейшего лечения отличия между группами по наиболее частым нежелательным явлениям исчезали.
Различные фармакологические характеристики и механизм действия α1-адреноблокаторов и ингибиторов 5α-редуктазы служат основой для разработки и применения рациональной комбинированной терапии. Комбинация аводарта (дутастерида) и тамсулозина изучалась в ходе 4-летнего, мультицентрового, рандомизированного исследования «слепым» методом «CombAT». В исследовании принимали участие параллельные группы из 4844 мужчин (средний возраст 50 лет) с клиническим диагнозом ДГП. Показатель по международной шкале проявлений заболеваний простаты составил более 12, объем простаты – более 30 смα, уровень ПСА – 1,5–10 мг/мл, максимальная скорость мочеиспускания (Qmax) – более 5–15 мл/с, минимальный объем выделенной мочи – 125 мг. Ежедневно перорально они принимали тамсулозин 0,4 г; дутастерид 0,5 мг или их совместную комбинацию. Первичной конечной точкой наблюдения в течение 4-х лет было возникновение острой задержки мочи или оперативное вмешательство по поводу доброкачественной гиперплазии простаты. Вторичными конечными точками исследования стал анализ клинической прогрессии ДГП, симптоматики, Qmax, объема простаты, безопасности и переносимости. Результаты комбинированной терапии намного превосходили монотерапию тамсулозином, но не монотерапию дутастеридом. Комбинированная терапия показала не только снижение относительного риска острой задержки мочи или оперативного вмешательства по поводу ДГП, но и значительно лучшие результаты относительно обеих монотерапий в сокращении риска клинической прогрессии ДГП. Данные, полученные в ходе 4-летнего исследования ComBat, говорят в поддержку использования комбинированной терапии тамсулозином и дутастеридом у мужчин с умеренными или выраженными СНМП, развившимися в связи с ДГП [12].
Литература
Сравнительная экспертиза препаратов на основе Тамсулозина
Мировые показатели рынка генериков
Отсутствие затрат на синтез новых молекул и клинические исследования делают производство генериков привлекательным способом участия небольших компаний в фармацевтическом бизнесе. Несомненно, подавляющее большинство компаний строго следят за всеми этапами производства ЛС. Однако на лекарственном рынке России, по мнению Хосевой Е.Н. (Оптимизация системы контроля эффективности и безопасности воспроизведенных лекарственных средств отечественного производства, 2014г), циркулирует от 20 до 40% фальсификата, который чаще всего характеризуется недовложением активного вещества. Возможность свободного приобретения рецептурных препаратов в аптеке без назначения врача, а только по советам знакомых и родственников, делает вдвойне опасным применение лекарств для здоровья и жизни пациентов.
Генерик (дженерик), согласно определению ВОЗ, представляет собой воспроизведенный лекарственный препарат, который обладает доказанной терапевтической взаимозаменяемостью с воспроизводимым оригинальным препаратом (препаратом-брендом). Предполагается, что генерики должны выпускаться иным производителем, нежели оригинальный препарат, после истечения срока патентной защиты, иметь более низкую стоимость, обусловленную отсутствием затрат на разработку уникальной формулы, дорогостоящие клинические исследования, а в ряде случаев и на маркетинговое продвижение и рекламу. Врач должен назначать генерик препарата только, если он уверен в его полной фармацевтической, биологической и терапевтической эквивалентности оригиналу.
Препараты на основе тамсулозина: сравнительная экспертиза
В 2018 году группой ученых из Институтов неорганической химии им. А.В. Николаева СО РАН и молекулярной и клеточной биологии СО РАН Новосибирска, при участии исследователей из Новосибирского Государственного университета, было проведено химико-фармакологическое исследование препаратов на основе тамсулозина – оригинального тамсулозина и 7 генерических аналогов. Целью данной работы было проведение сравнительного исследования технологических и физико-химических характеристик препаратов на основе тамсулозина гидрохлорида, используемых в настоящее время в России, для выявления отличий, а также возможных нарушений технологии производства, т.е. соответствия препаратов оригинальной модели и выявление отклонений, потенциально приводящих к изменению терапевтических свойств препарата.
Для достижения поставленной цели была проведена сравнительная экспертиза технологических показателей капсул:
Исследовались общие характеристики таблеток, морфология пленочного покрытия и материала ядра таблеток, состояние и химический состав материала таблеток, поведение таблеток и их ядер в тестах распадаемости, изучение осадка морфологии и фазового состава осадков.
Исследуемые показатели
Модель доставки тамсулозина также складывается из 3х компонентов:
В связи с этим исследователи провели анализ следующих показателей:
Изменение параметров любого из компонентов данной сложной сбалансированной системы «действующее вещество – лекарственная форма» приведет к изменению всей модели и требует изменения дизайна остальных компонентов для сохранения аналогичных с оригинальными фармакокинетических свойств препарата.
Результаты исследований эквивалентности
Омник
Исследование оригинального препарата Омник выявило полное соответствие физико-химических свойств капсул заявленному дизайну и составу. Исследование профиля высвобождения продемонстрировало постепенное высвобождение в установленные нормативные сроки согласно стандартам.
Фокусин
Исследование дженерического препарата Фокусин не выявило выраженных отклонений физико-химических свойств и состава капсул. Однако при исследовании профиля высвобождения были установлены выраженные отклонения: за первые 2 часа высвобождается недостаточное количество тамсулозина, а за 12 часов – избыточное. Таким образом, нарушаются первые два условия терапевтического воздействия препарата.
Профлосин
Исследование дженерического препарата Профлосин выявило изменение распределение размера гранул по сравнению с оригинальным препаратом: широкое, неравномерно распределение гранул различного размера со снижением среднего количества гранул в капсуле. Профиль высвобождения не соответствовал нормативам и был схож с профилем препарата Фокусин: за первые 2 часа высвобождается недостаточное количество тамсулозина, а за 12 часов – избыточное. Таким образом, имеются отклонения в компоненте К2 модельного препарата и нарушаются первые два условия терапевтического воздействия препарата.
Тулозин и Омсулозин
Исследование дженерических препаратов Тулозин и Омсулозин выявило значительное снижение среднего количества гранул в капсулах (более, чем в 4 раза), а в случае Тулозина – неравномерное распределение по размерам. Профиль высвобождения для обоих препаратов значительно отличался от нормативного – за 8 часов происходило полное высвобождение тамсулозина. Таким образом, имеются отклонения в компоненте К2 модельного препарата и нарушаются первые два условия терапевтического воздействия препарата.
Тамсулозин КАНОН
Исследование дженерического препарата Тамсулозин КАНОН выявило значительные изменения в составе, размерах и свойствах пеллетов. Замена инертной основы пеллетов с МКЦ на сахарозу привело к значительному изменению растворимости препаратов при низких значениях pH (отклонения в компоненте К3). Гранулы имеют неоднородное строение в направлении от центра к поверхности (отклонения в компоненте К3), их количество снижено (более, чем в 5 раз), а распределение по размерам имеет только 2 выраженных пика (отклонения в компоненте К2). Профиль высвобождения резко отличался от нормативного – за 4 часов происходило полное высвобождение тамсулозина. Таким образом, имеются отклонения в компонентах К2 и К3 модельного препарата и нарушаются первые два условия терапевтического воздействия препарата.
Тамсулозин (Вертекс)
Исследование дженерического препарата Тамсулозин (Вертекс) выявило значительные изменения в составе, размерах и свойствах пеллетов. Замена инертной основы пеллетов с МКЦ на сахарозу привело к значительному изменению растворимости препаратов при низких значениях pH (отклонения в компоненте К3). Количество гранул в капсулах резко снижено (более, чем в 7 раз) при узком распределении по размерам (отклонения в компоненте К2). Действующее вещество локализовано только в оболочке гранул (отклонения в компоненте К3). Изменена структура гранул – однородная плотная структура с наличием небольшого количества полостей (отклонения в компоненте К3). Исследования профиля высвобождения показало, что, хотя за первые 2 часа количество высвобождаемого тамсулозина находиться в пределах нормы, за 4 часа происходит полное высвобождение действующего вещества. Таким образом, имеются отклонения в компонентах К12 и К3 модельного препарата и нарушаются первые два условия терапевтического воздействия препарата.
Тамсулозин-OBL
Исследование дженерического препарата Тамсулозин-OBL выявило значительные изменения в составе, размерах и свойствах пеллетов. Замена инертной основы пеллетов с МКЦ на сахарозу привело к значительному изменению растворимости препаратов при низких значениях pH (отклонения в компоненте К3). Количество гранул в капсулах резко снижено (более, чем в 8 раз) при узком распределении по размерам (отклонения в компоненте К2). Действующее вещество локализовано только в оболочке гранул (отклонения в компоненте К3). Гранулы имеют неоднородное строение в направлении от центра к поверхности (отклонения в компоненте К3). Профиль высвобождения по 2 точкам из четырех не соответствовал нормативному. Кроме того, только для данного дженерического препарата было зафиксировано отклонения плоскости поляризации, что может свидетельствовать о нарушениях в энантиомерном составе препарата и требует дополнительного исследования. Таким образом, имеются отклонения в компонентах К2 и К3 модельного препарата, нарушаются первые два условия терапевтического воздействия препарата и есть основания предполагать возможные нарушения третьего условия терапевтического воздействия препарата.
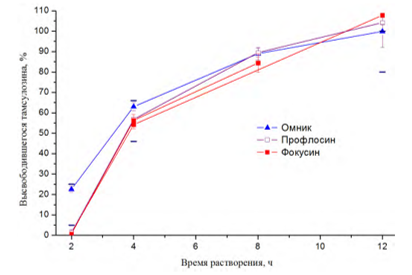
Рис. 1. Сравнение профилей высвобождения препаратов Омник, Профлосин, Фокусин, полученных исследователями. Рекомендованные параметры высвобождения тамсулозина отмечены темно-синими штрихами.
Вывод
Сводные результаты исследования представлены в таб. 1.
Препараты Омник, Фокусин, Профлосин соответствуют заявленному дизайну изготовления.
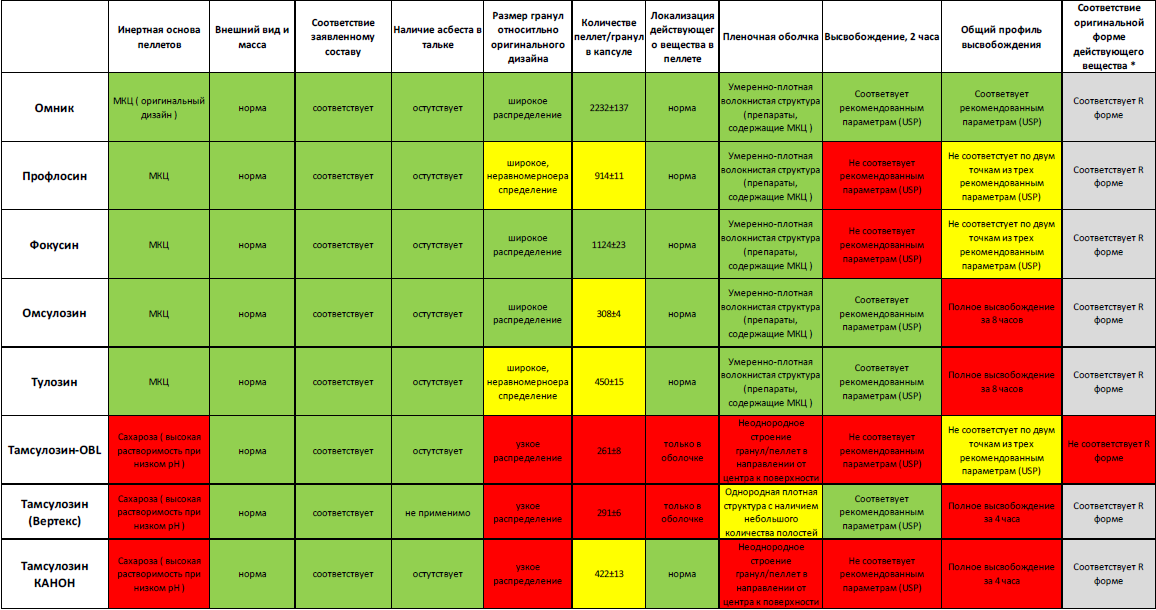
Табл. 1. Сводная таблица результатов исследования
Для препаратов Тулозин и Омсулозин выявлено ярко выраженное снижение количества гранул, которое требует изменения ряда физико-химических параметров для достижения необходимого профиля высвобождения.
Для группы препаратов Тамсулозин КАНОН, Тамсулозин (Вертекс) и Тамсулозин-OBL произведено серьезное изменение строение и состава гранул, что является предпосылкой к серьезным нарушениям в профилях растворения.
Согласно полученным результатам, следует ожидать существенное снижение терапевтического эффекта у препаратов Тамсулозин КАНОН, Тамсулозин (Вертекс), Тулозин и Омсулозин.
Согласно полученным результатам терапевтический эффект от препаратов Фокусин, Профлосин не ясен, но в силу неэквивалентности профилей высвобождения требуемым стандартам, можно сделать заключение об отсутствии физико-химической, и, как следствие, терапевтической эквивалентности с оригинальным препаратом, соответствующим стандарту.
В случае исследованных дженериков тамсулозина исследователям не удалось обнаружить в научной литературе статей по разработке нового дизайна препарата с замедленным высвобождением ни для одного из них.
Материал подготовлен научным редактором Uroweb.ru
В.А. Шадеркиной
1. Хосева Е.Н. Оптимизация системы контроля эффективности и безопасности воспроизведенных лекарственных средств отечественного производства. Авт. докт. диссерт. Москва, 2014. (про фальсификат)
