что лучше таурин или метформин
Дефицит таурина в России и его последствия. Эффекты Дибикора в клинике
Опубликовано в:
«СПРАВОЧНИК ПОЛИКЛИНИЧЕСКОГО ВРАЧА» »» 2011 № 8
Е.П.Елизарова, Е.В.Доскина
Кафедра эндокринологии и диабетологии с курсом эндокринной хирургии РМАПО, Москва
Обзор
На основании многочисленных экспериментальных данных, подтверждающих благоприятный эффект таурина и других нутриентов в профилактике сердечно-сосудистых заболеваний (ССЗ), Y.Yamori в 1982 г. предложил провести международное кооперативное исследование ассоциации особенностей характера питания, факторов риска ССЗ и сердечно-сосудистой смертности. Протокол исследования был одобрен международным экспертным комитетом на двух заседаниях, организованных Центром Всемирной организации здравоохранения по первичной профилактике ССЗ в 1983 и 1985 гг.
Исследование CARDIAC являлось многоцентровым одномоментным эпидемиологическим исследованием, в которое вошли 100 мужчин и 100 женщин 48-56 лет, методом случайной выборки отобранные из 61 популяции. Исследование длилось с 1985 по 2005 г.
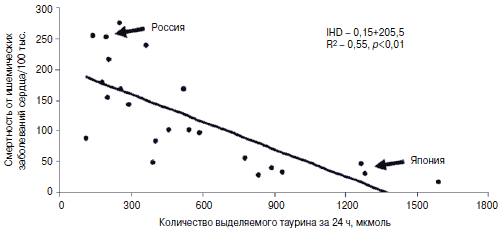
Многие факты, которые давно известны научному медицинскому обществу (корреляция смертности при ишемической болезни сердца от индекса массы тела, K + в моче, пальмитиновой кислоте в фосфолипидах и т.д.), подтвердились. Между тем, были получены и новые результаты, в частности, что смертность от ишемической болезни сердца обратно пропорциональна количеству выделяемого с мочой таурина. На рис. 1 представлены данные этой зависимости. Стрелками указаны точки, которые соответствуют средним значениям выделения таурина у жителей нашей страны и Японии.
Рис 1. Корреляция между смертностью от коронарной болезни сердца на 100 тыс. населения и выделением таурина с мочой.
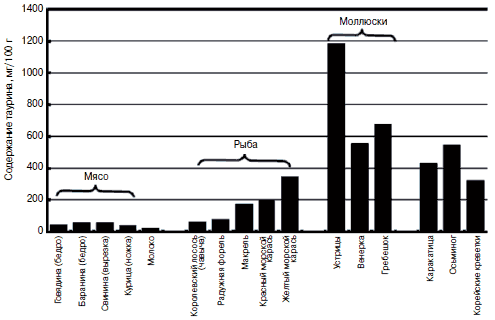
Рис. 2. Содержание таурина в продуктах.
Как видно из рис. 2, содержание таурина в традиционной для России пище очень низкое. Уровень потребления и выделения таурина в России невелик из-за удаленности основного населения от морских побережий.
Во многих странах таурин используется в качестве нутриента. По уровню доказательности для лечения кардио-васкулярных заболеваний его отнесли к уровню «В». В нашей стране на основе таурина выпускается лекарственный препарат Дибикор ® (таурин) в таблетках по 0,5 и 0,25 г. Он прошел как доклинические, так и клинические исследования.
Эффекты Дибикора в клинике
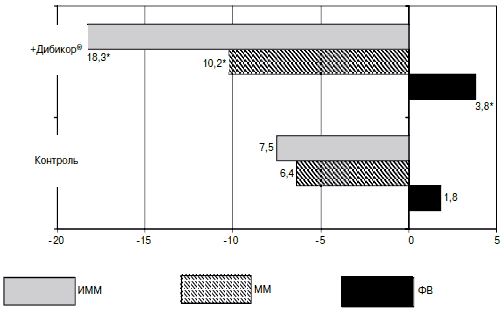
Эффекты Дибикора при лечении хронической сердечной недостаточности (ХСН) с метаболическим синдромом изучались в Кубанском государственном медицинском университете. Все больные (общее количество 60 человек) были рандомизированы в 2 группы по 30 больных и находились на терапии эналаприлом и индапамидом. К опытной группе добавляли Дибикор ® (0,5 г 2 раза в день). Курс лечения 12 мес. Динамика показателей ремоделирования миокарда левого желудочка приведена на рис. 3.
Рис. 3. Изменение индекса массы миокарда, массы миокарда, фракции выброса.
Примечание. *р ® проявляет профилактические свойства у этих больных.
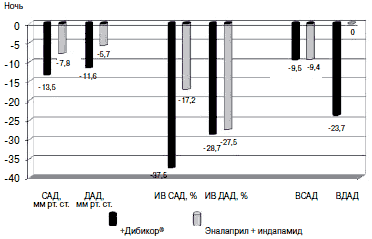
Рис. 4. Динамика показателей СМАД у больных с ХСН и метаболическим синдромом, терапия Дибикором.
Эффекты Дибикора при лечении сахарного диабета типа 2
В табл. 1, 2 приводятся результаты исследований, которые прошли в двух независимых медицинских центрах (ГОУ ДПО Санкт-Петербургская МАПО Федерального агентства по здравоохранению и социальному развитию, ФГУ ЭНЦ Росмедтехнологий).
Таблица 1. Динамика показателей углеводного обмена у больных основной и контрольной групп
| Показатель | Основная группа | Контрольная группа | |||||
| до исследования | после | Р | до исследования | после | Р | ||
| Гликемия тощаковая, моль/л | МАПО ЭНЦ | 8,9±0,33 9,57±1,68 | 7,2±0,24 7,83±0,88 | 0,00004 0,00007 | 8,7±0,16 8,52±1,64 | 8,2±0,20 8,11±1,04 | 0,169 0,13 |
| HbA1c, % | МАПО ЭНЦ | 8,4±0,21 8,16±0,86 | 7,2±0,14 7,73±0,60 | 0,00004 0,002 | 8,3±0,12 8,18±1,15 | 8,3±0,16 8,13±1,16 | 0,332 0,17 |
Таблица 2. Динамика показателей липидного обмена у больных основной и контрольной групп
Добавление Дибикора к стандартной терапии улучшило показатели углеводного обмена (см. табл. 1). По результатам исследований в МАПО и ЭНЦ показано, что с большой степенью достоверности уменьшилась гликемия тощаковая и гликозилированный гемоглобин. В контрольной группе в обоих центрах, несмотря на интенсивную терапию, положительных сдвигов этих показателей получить не удалось.
Эффективность Дибикора при лечении больных сахарным диабетом (СД) и ХСН подтверждается и другими многочисленными исследователями, прошедшими в Российской Федерации. Это не все эффекты, которые наблюдаются при терапии Дибикором. Так, было замечено, что Дибикор ® уменьшает выделение мочевой кислоты, уменьшает АСТ/АЛТ.
Почему добавление Дибикора столь значимо компенсирует течение СД? Дефицит таурина в питании, который наблюдается у нашего населения, более усиливается при СД. Практически в 2 раза падает концентрация таурина в клетках крови и в плазме у пожилых людей. Некоторые препараты и стресс также способствуют выведению таурина из организма. Дефицит таурина в любом органе создает проблемы, которые могут решаться только устранением этого дефицита. Заменить таурин другим веществом нельзя, так как таурин затрагивает много физиологических и биохимических процессов в клетке. Он является основным осмо-регулятором, мембранным протектором, модулятором внутриклеточного кальция. У него найдены антиоксидантные свойства. Таурин, как показали последние исследования, влияет на синтез и сборку белков дыхательной цепи митохондрий. По всей видимости, комплексная терапия не приводит к желаемым результатам именно из-за недостаточности таурина у больных, а устранение дефицита таурина препаратом Дибикор ® улучшает метаболические процессы, которые мы констатируем по улучшению углеводного и липидного обмена и по изменению гемодинамики и функциональной активности сердца. Влияние Дибикора на артериальное давление также представляется следствием действия препарата на общий обмен веществ.
Поскольку наше население лишено продуктов, богатых таурином, Дибикор ® может решить проблему недостатка таурина в питании. Отсутствие у Дибикора побочных эффектов и противопоказаний, совместимость с другими препаратами делает его незаменимым при добавлении к терапии целого ряда заболеваний, сопряженных с нарушением обмена веществ.
Эффективность и переносимость таурина у пациентов с сахарным диабетом 2-го типа и диастолической дисфункцией левого желудочка
Диастолическая дисфункция (ДД) регистрируется у пациентов с сахарным диабетом 2-го типа (СД 2-го типа) без сопутствующей сердечно-сосудистой патологии в 50–75% случаев [1, 2] и рассматривается исследователями как проявление диабетической кардиомиопатии [3
Диастолическая дисфункция (ДД) регистрируется у пациентов с сахарным диабетом 2-го типа (СД 2-го типа) без сопутствующей сердечно-сосудистой патологии в 50–75% случаев [1, 2] и рассматривается исследователями как проявление диабетической кардиомиопатии [3]. В патогенезе последней участвует множество факторов, ассоциированных с течением диабета, наиболее изученными из которых являются повреждающее действие гипергликемии, конечных продуктов гликирования и реактивных форм кислорода, феномен липотоксичности, а также эндотелиальная дисфункция. Частота регистрации ДД увеличивается при наличии сопутствующих заболеваний сердечно-сосудистой системы, в частности, у пациентов с СД 2-го типа и артериальной гипертензией (АГ) частота выявления ДД может достигать 85% [4]. В связи с этим изучение возможностей профилактического и/или лечебного воздействия в контексте ДД, как одного из наиболее ранних маркеров формирования хронической сердечной недостаточности, остается актуальным. В течение последних 20 лет в мировой литературе накапливаются данные о перспективах применения у пациентов с СД таурина — 2-аминоэтансульфоновой кислоты, широко представленной в миллимолярных концентрациях в тканях млекопитающих. Таурин поступает в организм с пищей и синтезируется из метионина и цистеина, главным образом, в печени [5]. Интересен факт, что таурин находится в высоких концентрациях в морской рыбе, являющейся его важнейшим источников для человека, и именно среди групп населения с высоким употреблением рыбы выявляются наиболее низкие показатели сердечно-сосудистой смертности [6]. Повышенное употребление таурина по некоторым данным обратно коррелирует с распространенностью ишемической болезни сердца (ИБС) [7]. По данным эпидемиологического исследования Yamori et al. (2001), уровень экскреции таурина, как показатель уровня его потребления, обратно коррелирует со смертностью от ИБС [8]. По некоторым данным плазменный уровень таурина у пациентов с СД ниже, чем в общей популяции [10, 11].
Предполагаемое на основании экспериментальных и клинических исследований позитивное влияние таурина на деятельность сердца (модуляция активности транспортеров кальция и чувствительности кардиомиоцитов к кальцию; участие в клеточной осморегуляции, непрямая регуляция внутриклеточных окислительных процессов (механизм неизвестен), стабилизация клеточных мембран (прямое взаимодействие с фосфолипидами), модуляция активности протеинкиназ и фосфатаз кардиомиоцитов) [18] ориентируют на продолжение клинических исследований в этом направлении.
Материал и методы
С целью изучения влияния таурина (Дибикор) на состояние углеводного обмена и липидного обменов, состояние сердечно-сосудистой системы, клинический статус и показатели качества жизни пациентов, страдающих СД 2-го типа, было обследовано 195 больных. В плацебо-контролируемое двойное слепое исследование были включены 80 пациентов с установленным диагнозом СД 2-го типа в соответствии с критериями включения (наличие ранее диагностированного СД 2-го типа; возраст больных 45–60 лет; письменное информированное согласие больного; пероральная сахароснижающая терапия; HbA1c 60 лет; инсулинотерапия; АГ, некоррегированная; ХСН 3 ст., ФК 3; постинфарктный кардиосклероз, острое нарушение мозгового кровообращения в анамнезе, хроническая почечная и/или печеночная недостаточность; HbA1c ≥ 7%; прием препаратов, способных потенциально повлиять на результаты лечения; невозможность по любым причинам участвовать в проспективном исследовании).
У всех больных проводилось изучение жалоб, данных анамнеза, полное физикальное обследование. Проводилось исследование состояния углеводного обмена (HbA1c; глюкоза крови натощак и постпрандиально в плазме капиллярной крови); липидного обмена (общий холестерин (ОХ), липопротеины низкой плотности (ЛПНП), очень низкой (ЛПОНП) и высокой плотности (ЛПВП), триглицериды (ТГ)). Оценка морфо-функционального состояния сердца осуществлялась по результатам ЭКГ (PORTRAIТ, MORTARA); ЭхоКГ (Aloka SSD-2000) с анализом показателей диастолической функции миокарда левого желудочка (пиковая скорость фазы раннего наполнения; пиковая скорость фазы предсердного наполнения; соотношение пиковых и спектральных скоростей раннего и предсердного наполнения между собой E/A; время изоволюметрического расслабления левого желудочка (IVRT); время замедления раннего трансмитрального потока (DT)). Для оценки качества жизни использовалась русифицированная версия опросника SF-36. Всем пациентам в ходе исследования проводилась коррекция лекарственной сахароснижающей терапии при необходимости для достижения/поддержания целевых значений HbA1c 2 ). Во всех процедурах статистического анализа рассчитывался достигнутый уровень значимости (p), при этом критический уровень значимости в данном исследовании принимался равным 0,05.
Результаты и обсуждение
Подробная клиническая характеристика пациентов, включенных в исследование, представлена в табл. 1.
Группы пациентов были сопоставимы по полу, возрасту, основным клиническим характеристикам.
На момент включения в исследование большинство пациентов обеих групп получали комплексное медикаментозное лечение, включающее сахароснижающие препараты и препараты для лечения сопутствующей сердечно-сосудистой патологии (табл. 2). При этом в группе 1 средняя суточная доза метформина в виде монотерапии составила 1,74 г/сут, в составе комбинированной терапии — 1,77 г/сут; среднесуточная доза глибенкламида (микронизированная форма препарата) — 6,71 мг/сут, гликлазида — 50 мг/сут; ситаглиптина — 100 мг/сут. В группе 2 средняя суточная доза метформина в виде монотерапии составила 1,83 г/сут, в составе комбинированной терапии — 1,54 г/сут; среднесуточная доза глибенкламида (микронизированная форма препарата) — 6,75 мг/сут, гликлазида — 52,11 мг/сут; ситаглиптина — 100 мг/сут.
Характер противодиабетической терапии не различался значимо между группами.
По данным ЭКГ у большинства пациентов регистрировались изменения процессов реполяризации миокарда: 1-й степени — 26 пациентов группы 1 и 23 пациента группы 2; 2-й степени — 12 и 15 пациентов, 3-й степени — 1 и 2 пациента (соответственно в группе 1 и группе 2). По данным ЭхоКГ у всех включенных в исследование пациентов регистрировалась ДД левого желудочка 1-го типа (замедление релаксации): IVRT > 100 мс при Е/А 250 мс.
Анализ полученных данных проводился исходя из допущения, что все больные получали предписанное лечение (собеседование во время каждого визита, 1 раз в месяц). Полный 16-недельный курс терапии закончили все пациенты.
Большинство пациентов обеих групп на момент включения в исследование предъявляли разнообразные жалобы со стороны сердечно-сосудистой системы: абсолютное большинство пациентов отмечали плохую переносимость физической нагрузки в связи с утомляемостью, сердцебиениями, одышкой, дискомфортом в области сердца. Большая часть пациентов испытывала ощущения сухости во рту, редкие эпизоды легких гипогликемических состояний, купировавшихся приемом углеводов и связанных, как правило, с нарушениями режима питания. Оценка динамики субъективного статуса пациентов осуществлялась на каждом визите, ежемесячно (табл. 3). В обеих группах за время наблюдения была отмечена некоторая положительная тенденция снижения частоты регистрации указанных жалоб. Однако достоверная статистическая динамика была зарегистрирована к окончанию периода наблюдения более отчетливо в группе 1 (уменьшение жалоб на утомляемость/усталость, сердцебиение, перебои в работе сердца, одышку, боли в сердце, сухость во рту).
В группе плацебо отмечено снижение частоты регистрации жалоб на боли в области сердца (р 0,05). Вместе с тем в группе 1 достоверно меньшее количество пациентов (р = 0,041) к моменту окончания исследования имели ИМТ, соответствующий ожирению 1–3 степени, в сравнении с группой плацебо (12/40 и 22/40 соответственно). Указанные изменения могут быть связаны с большей приверженностью пациентов группы 1 рекомендациям по повышению двигательной активности в связи с зарегистрированным улучшением субъективной переносимости физических нагрузок.
За время наблюдения на фоне сахароснижающей терапии положительных тенденций изменения МТ в обеих группах было отмечено некоторое снижение показателей уровня глюкозы плазмы капиллярной крови (табл. 4). В группе 1 отмечено достоверное снижение показателей гликемии натощак и постпрандиально. В группе плацебо снижение гликемии натощак было несколько более выражено в сравнении с изменением постпрандиального уровня, однако указанная тенденция не была статистически значима (p > 0,05), была отмечена статистически незначимая тенденция к повышению уровня гликемии постпрандиально.
Долгосрочное влияние препарата на показатели углеводного обмена (HbA1c) было достоверно установлено в группе 1 в виде статически значимого умеренного снижения (табл. 4), в то время как в группе плацебо отмечена тенденция к некоторому ухудшению контроля гликемии (тенденция повышения уровня HbA1c, однако, не достигла статистически достоверного уровня).
Кроме того, адекватный контроль заболевания (HbA1c 0,05).
ЭхоКГ-параметры пациентов обеих групп в целом не претерпели существенных изменений (табл. 5). В группе 1, в отличие от группы 2, отмечено достоверное повышение среднего по группе показателя Е/А на фоне снижение IVRT, что в целом явилось отражением нормализации диастолической функции сердца у большинства пациентов.
Было зарегистрировано достоверное уменьшение частоты регистрации ДД в группе 1 (рис. 2).
.gif)
.gif)
.gif)
_500.gif)
.gif)
_500.gif)
 Только при сахарном диабете 2 типа могут использоваться лекарственные препараты, а не инсулин.
Только при сахарном диабете 2 типа могут использоваться лекарственные препараты, а не инсулин. Глифлозины уменьшают частоту госпитализаций при хронической сердечной недостаточности.
Глифлозины уменьшают частоту госпитализаций при хронической сердечной недостаточности.