элидел или такропик что лучше
Элидел и кортикостероиды: союзники или соперники?
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
МГУ им. М.В. Ломоносова, ЦКБ, Москва
Н аружные кортикостероиды (КС) являются основой лечения атопического дерматита (АД), так как обладают противовоспалительными, иммуносупрессивными и антипролиферативными свойствами. Эти препараты действуют быстро и эффективно, что удовлетворяет и врача и больного. Вместе с тем стероиды обладают целым рядом серьезных побочных эффектов. Особенно опасны системные осложнения, развивающиеся, как правило, вследствие всасывания препаратов у очагов поражения большой площади при длительном применении. Группой риска №1 в этом отношении являются дети до 2 лет, у которых проницаемость кожи гораздо выше, чем у взрослых [1]. К наиболее грозным системным осложнениям относят угнетение гипоталамо–гипофизарно–адреналовой системы и связанные с этим задержку роста, синдром Кушинга, гипертензию, диабет [2–6]. Длительное использование местных стероидов сопряжено с риском иммуносупрессии, что проявляется бактериальной, вирусной и грибковой инфекцией. Преимущественно эти эффекты характерны для ранних поколений КС, особенно фторированных КС. В последние десятилетия созданы препараты, всасываемость которых при наружном применении не превышает 1%, однако и они обладают целым рядом недостатков. Среди местных осложнений преобладает атрофия кожи, стрии, телеангоэктазии, нарушения пигментации, акнеиформные высыпания [7]. К важным недостаткам наружных КС относится и тахифилаксия – привыкание и утрата эффективности.
Все эти побочные эффекты и осложнения привели тому, что 73% больных АД страдают так называемой «стероидной фобией» – беспокойством разной степени, вплоть до полного отказа от применения КС [8]. По этой причине 24% взрослых пациентов и 36% родителей больных детей признаются в нарушении режима наружной терапии. «Стероидной фобией» страдают не только пациенты, но и сами врачи, поэтому зачастую лечение этими препаратами начинают применять с опозданием, длительность терапии недостаточна, а дозы, особенно у детей, слишком малы. Все это приводит к неполноценному купированию обострения, раннему рецидиву и формированию тахифилаксии.
В этой связи возникает вопрос: как сократить срок использования КС при обострении АД и вместе с тем продлить ремиссию заболевания?
Для решения этой проблемы в настоящее время используется селективный ингибитор синтеза и высвобождения провоспалительных цитокинов – пимекролимус (SDZ ASM 981). Установлено, что это вещество In vitro избирательно связывается с макрофилином–12, и ингибирует кальциневрин и тем самым – синтез воспалительных цитокинов в Т–клетках (ИЛ–2, INF–g), а также высвобождение медиаторов воспаления (например, гистамина) из тучных клеток [9–12]. В то же время пимекролимус не влияет на кератиноциты, фибробласты, эндотелиальные клетки и клетки Лангерганса. In vivo препарат обладает высокой противовоспалительной и незначительной иммуносупрессивной активностью [9–12], не вызывает атрофии [13]. Пимекролимус обладает высоким сродством к коже, поэтому хорошо пенетрирует внутрь нее и практически не проникает через кожу [11].
Клиническими испытаниями установлена безопасность и эффективность 1% крема пимекролимуса – Элидела® (фирма Novartis, Швейцария) при его кратковременном и длительном применении у детей и взрослых, больных АД.
Для того, чтобы попытаться сократить с помощью Элидела частоту и длительность рецидивов и зависимость пациентов от наружных КС при АД у взрослых было проведено многоцентровое рандомизированное контролируемое исследование двойным слепым методом длительностью 24 недели [14].
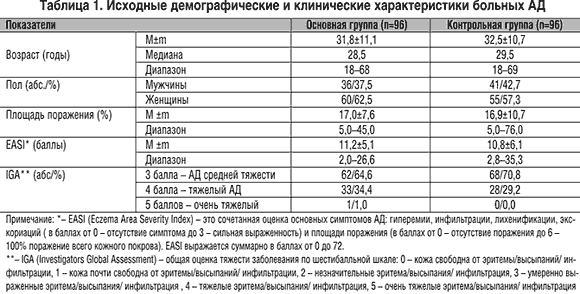
Наблюдали 192 больных АД в возрасте от 18 лет и старше. Диагноз установлен в соответствии с критериями Hanifin [15] и Rajka [16]. Площадь поражения до начала лечения составляла не менее 5%, в среднем – 17% в обеих группах. В каждой группе преобладали больные АД средней тяжести (по шкале IGA – 3 балла).
По результатам рандомизации 96 пациентов были включены в основную, 96 – в контрольную группу. Статистически значимых демографических и клинических различий между группами не было (табл. 1).
Пациенты основной группы получали наружное лечение кремом Элидел 2 раза в сутки, контрольной – только основу крема. В первую неделю исследования такая схема лечения была обязательной. В дальнейшем в случае развития обострения назначались наружные КС (предникарбат 0,25% крем) два раза в сутки в течение 7 дней и один раз в сутки – в течение следующей недели. После терапии КС лечение исследуемым препаратом проводилось еще в течение 1 недели для купирования остаточных явлений обострения (табл. 2).
Основным критерием эффективности было количество дней (%), в течение которых КС применялись для неотложной терапии обострения. Дополнительную оценку эффективности проводили по следующим параметрам: количество обострений, результаты IGA, EASI, интенсивность зуда. Последний параметр оценивали сами пациенты, используя следующую шкалу в баллах: 0 – отсутствие зуда, 1 – незначительный зуд, 2 – умеренный зуд, 3– сильный зуд, 4 – очень сильный зуд. Переносимость оценивали по клиническим и лабораторным данным.
Обследование пациентов проводили во время первичного осмотра, а затем на 1, 3, 6, 12 и 24–й неделях лечения. Кроме этого, осуществляли дополнительный телефонный контакт на 9 и 18–й неделях. В случае сильного обострения проводили незапланированные осмотры.
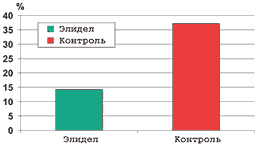
В основной группе пациентов, получавших лечение кремом Элидел, зарегистрировано статистически достоверное (по сравнению с контрольной группой) уменьшение количества дней, в течение которых пациенты вынуждены были применять КС (рис. 1).
Рис. 1. Количество дней, в течение которых пациенты использовали кортикостероиды (%)
В основной группе пациенты использовали КС в среднем в течение 14,2%±24,2% из 168 дней (общая продолжительность исследования), а в контрольной – в 37,2%±34,6% (р Рис. 2. Количество дней, когда пациентам требовалось лечение местными кортикостероидами (%)
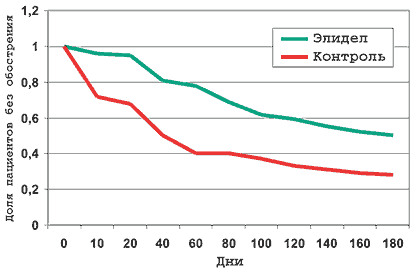
Частота обострений и время до наступления первого обострения также значимо различались между двумя группами пациентов. В основной группе в среднем зарегистрирован 1,1±1,4 случай обострения, в контрольной – 2,4±2,3 (р Рис. 3 Частота обострений (%)
Рис. 4. Время до первого обострения
При оценке по шкале IGA у 82.3% пациентов основной группы отмечено улучшение по крайней мере на один балл против 51,0% – в контрольной, а показатель EASI снизился в среднем на 48.3% против 15,9% (соответственно) (р Рис. 5. Динамика зуда в течение первой недели лечения
Крем Элидел хорошо переносился больными, патологии традиционных лабораторных анализов на протяжении всего исследования ни у кого из пациентов не выявлено.
Таким образом, наружное лечение больных АД кремом Элидел позволяет:
1. Giusti F, Martella A, Bertoti L, Seidenari S. Skin Barrier, Hydration, and pH of the Skin of infants under 2 years of age. Ped Derm 2001; 18: 93–6.
2. Keipert JA, Kelly R. Temporary Cushing’s syndrome from percutaneous absorption of betamethasone–17–valerate. Med J Austr 1971; 1: 542–4.
3. Pascher F. Systemic reactions to topically applied drugs. Int Dermatol 1978; 17: 768–75.
4. Bode HH. Dwarfish following long long–term topical corticosteroid therapy. J M Med Assoc 1980; 244: 813–14.
5. Bartorelli A, Rimondini A. Severe hypertension in childhood due to prolonged skin application of mineralocorticoid ointment. Hypertension 1984; 6: 586–8.
6. Walsh P, Aeling JL, Huff L, Weston WL. Hypothalamus–pituitary–adrenal axis suppression by superprotent steroids. J Am Acad Dermatol 1999; 29: 501–3.
7. Fisher DA. Adverse effects of topical corticosteroid use. West J Med 1995; 162: 123–6.
8. Charman C, Morris A, Willians H. Topical corticosteroid phobia in patients with atopic dermatitis. Br J Dermatol 2000;142: 931–6.
9. Meingassner JG, Grassberger M, Fahrngruber H et al. A novel anti–inflammatory drug, SDZ ASM 981, for the topical and oral treatment of skin diseases: in vivo pharmacology. Br J Dermatol 1997; 137: 568–76.
10. Grassberger M, Baumruker T, Enz A et al. A novel anti–inflammatory drug, SDZ ASM 981, for the treatment of skin diseases: in vitro pharmacology. Br J Dermatol. 1999 Aug;141(2):264–73
11. Stuetz A, Grassberger M, Meingassner JG. Pimecrolimus (Elidel(, SDZ ASM 981) – Preclinical pharmacological profile and skin selectivity. Seminars Cutan Med Surg 2001; 20(4):233–41.
12. Zuberbier T, Chong SU, Grunow K et al. The ascomycin macrolactam pimecrolimus (Elidel, SDZ ASM 981) is a potent inhibitor of mediator release from human dermal mast cells and peripheral blood basophils. J Allergy Clin Immunol. 2001 Aug; 108(2): 275–80.
13. Queille–Roussel C, Paul C, Duteil L et al. The new topical ascomycin derivative SDZ ASM 981 does not induce skin atrophy when applied to normal skin for 4 weeks: a randomized, double–blind controlled study. Br J Dermatol. 2001 Mar; 144(3): 507–13.
14. Meurer M, Folster–Holst R, Brautigam M. Pimecrolimus (SDZ ASM 981) cream reduces the need for corticosteroids in the long–term management of atopic dermatitis in adults. Study, presented at the 60–th annual meeting of the American Academy of Dermatology in New Orleans, USA, February 2002
16. Rajka G. Natural history and clinical manifestations of atopic dermatitis. Clin Rev Allergy. 1986 Feb; 4(1): 3–26.
Локальная противовоспалительная терапия при атопическом дерматите: современный подход
В XXI в. произошли существенные изменения в изучении атопического дерматита (АД): новейшие методы молекулярной генетики и биологии, междисциплинарный подход, активная научно-исследовательская работа способствовали прогрессу медицины в области патофизиолог
В XXI в. произошли существенные изменения в изучении атопического дерматита (АД): новейшие методы молекулярной генетики и биологии, междисциплинарный подход, активная научно-исследовательская работа способствовали прогрессу медицины в области патофизиологии и терапии этого заболевания.
Наиболее важные достижения, а также соответствующие рекомендации по лечению и профилактике АД были сформулированы экспертами США и Европейского Союза (ЕС) в согласительном документе «Диагностика и лечение атопического дерматита у детей и взрослых» в 2006 г. [1]. В нем определение заболевания звучит коротко: «АД — хроническое воспалительное заболевание кожи, сопровождающееся зудом». Международная группа ученых рекомендует врачам при планировании лечения больных с АД использовать ступенчатый подход (рис.).
Как видно из представленной схемы, на всех стадиях течения АД больным показано основное лечение, которое включает соответствующий уход за кожей (очищение и гидратацию кожи с помощью увлажняющих/смягчающих средств и исключение/снижение влияния провоцирующих факторов), на фоне которого в дальнейшем назначают противовоспалительные препараты.
Уход за кожей основан на применении особых лечебных средств, достаточно широко представленных на современных фармацевтических рынках России. Местная противовоспалительная терапия включает всего лишь две группы лекарств — топические глюкокортикостероиды (ТГКС) и топические ингибиторы кальциневрина (ТИК). При осложнениях АД бактериальной/грибковой/вирусной инфекциями лечение следует продолжить наружными комбинированными или системными препаратами.
Системную терапию (антибиотики, пероральные кортикостероиды, циклоспорин А, азатиоприн, антигистаминные препараты) назначают больным с тяжелой формой АД, имеющим упорно рецидивирующее течение и/или другие сопутствующие заболевания. Взрослым и детям в возрасте старше 12 лет, страдающим тяжелым течением АД, возможно использование фототерапии. В последнее время рассматривается также целесообразность применения аллерген-специфической иммунотерапии в лечении АД.
Наружная (топическая) терапия является патогенетически обоснованной и абсолютно необходимой для каждого пациента с АД. Такая принципиальная важность топической терапии при АД объясняется несколькими факторами. Во-первых, АД — это хронический воспалительный процесс, который протекает в дерме, поэтому главное место в лечении заболевания должна занимать наружная терапия. Во-вторых, при АД крайне важно достичь восстановления и поддержания целостности кожного барьера, нарушение которой является кардинальным признаком АД, влекущей за собой усиление трансэпидермальной потери воды, а также повышение чувствительности кожи к различным ирритантам и аллергенам [3, 4]. Другим важным подходом является воздействие на сухость (ксероз) кожи при АД. Иными словами, наружная терапия — это именно тот вид лечения, который может изменить течение и исход АД.
Рассмотрим некоторые особенности наружной терапии АД, основанной на поэтапном подходе (рис.). Совершенно очевидно, что прежде следует оценить тяжесть течения заболевания.
Оценка степени тяжести АД
АД, как правило, начинается в раннем детском возрасте. Согласно последней классификации, различают не-атопическую и атопическую формы АД (в англоязычной литературе АД обозначают термином «экзема») (2001). По данным зарубежных исследователей, у 30–50% детей с типичной клинической картиной АД не удается подтвердить наличие атопических механизмов; у 15–45% детей описана преходящая (транзиторная) форма АД с низкими сывороточными уровнями IgE, не сопровождающаяся явной сенсибилизацией [2]. Позднее некоторые случаи так называемой eczema infantum спонтанно разрешаются без развития типичного АД. У другой части детей, напротив, заболевание характеризуется формированием сенсибилизации. Недавно Novembre E. с соавторами, исследовав 111 детей в возрасте 2–11 лет, установили, что по данным кожных прик-тестов лишь через 9 лет более чем у половины из них отрицательные кожные пробы стали положительными [3].
К сожалению, не существует потенциальных и объективных маркеров, которые отражали бы степень тяжести и прогрессирования заболевания и которые могли бы быть использованы для оценки эффективности терапии.
В клинической практике для оценки степени тяжести течения АД чаще всего врачи используют такие критерии, как выраженность эритемы, инфильтрации, папулы (индексы IGA — Investigator’s Global Assessment, EASI — Eczema Area Severity Index), еще раньше с этой целью был предложен индекс SCORAD (Scoring Atopic Dermatitis), рекомендованный Европейской академией аллергологии и клинической иммунологии в 1992 г. (данная система учитывает распространенность кожного процесса, интенсивность клинических проявлений и субъективные симптомы).
Вместе с тем, диагноз АД — прежде всего клинический. Основные подходы к наружной терапии при обеих формах АД одинаковы и ставят своей целью увлажнение/смягчение кожи и облегчение зуда. Лечение сухости кожи у больных АД проводят постоянно, тогда как выбор противовоспалительных средств зависит от степени тяжести течения заболевания.
Увлажняющие/смягчающие средства
Тот факт, что сухость (ксероз) и дефекты барьерной функции кожи влияют на течение АД, вполне очевиден. В результате многих исследований установлено, что существует взаимосвязь между зудом, сухостью и воспалением кожи, однако, что первично в этих процессах, точно не ясно. В последнее время дефекты барьерной функции кожи рассматривают как один из важных фенотипических признаков АД, который приводит не только к ксерозу, но и к снижению уровня антимикробных пептидов в коже и повышению трансэпидермальной потери воды. Но одни ученые рассматривают нарушение эпидермального барьера кожи как первичное звено в развитии АД, что способствует облегчению проникновения аллергенов и ирритантов в кожу, впоследствии инициирующих воспалительный ответ и гиперреактивность кожи. Другие, напротив, полагают, что нарушение барьерной функции кожи является вторичным процессом вследствие воспаления, которое развивается в ответ на проникновение аллергенов и ирритантов в кожу [4].
Нарушение барьерной функции кожи имеет место при обоих типах АД — атопическом и неатопическом (при последнем, возможно, оно выражено в большей степени). Доказано также, что при АД кожа сухая даже вне обострения заболевания [1–3]. В связи с этим обосновано применение увлажняющих/смягчающих средств и в те периоды заболевания, когда его симптомы отсутствуют.
На что влияет сухость кожи? Установлено, что при наличии ксероза восприимчивость кожи к экспозиции окружающих аллергенных и неаллергенных раздражителей, ирритантов, а также бактерий и вирусов существенно повышается. Следует учитывать также тесную взаимосвязь цикла «ксероз–зуд». Кроме того, при сухости кожи отмечается усиление системной абсорбции ТГКС, следовательно, и их побочных действий [5].
Из этих данных следует, что эффективное воздействие на сухость, зуд кожи, а также дефекты ее барьерной функции будет способствовать повышению результатов терапии АД. Однако повлиять на такие причины возникновения ксероза, как изменения в роговом слое, нарушения кератинизации, состава баланса внутриклеточных липидов, метаболизма трансэпидермальной воды, изменения рН кожи и т. п. — весьма сложная задача. Кроме того, ксероз и дефекты барьерной функции кожи характеризуются различными биохимическими, физико-химическими и морфологическими изменениями.
Разработан целый ряд специальных лечебных средств ухода за сухой и атопической кожей. В России в настоящее время доступны очищающие и увлажняющие/смягчающие средства различных лечебно-косметических линий: «Топикрем», «Авен», «Мустела Стелатопия», «Урьяж Cu-Zn», «Биодерма», «Дардия», «Виши» и т. п. При их использовании следует учитывать: полноту серии; возраст, с которого можно использовать наружное средство; способность средства создавать защитную пленку на коже, подавлять рост микроорганизмов; восстанавливать липидный слой в коже; противовоспалительный эффект и т. д. Эффективность увлажняющих/смягчающих средств зависит от дозы (их следует применять регулярно и в достаточном количестве), рН кожи, а также от комплаентности больных.
Локобейз Рипеа ® также содержит наночастицы твердого парафина, которые повышают его эффективность, удлиняют время действия и улучшают косметические свойства крема.
Как показывают клинические исследования, за счет восстановления и поддержания нарушенной барьерной функции кожи у пациентов с АД Локобейз Рипеа ® ускоряет разрешение симптомов обострения, повышает эффективность ТГКС и уменьшает потребность в их применении.
Локобейз Рипеа ® не содержит красители, отдушки и консерванты, что минимизирует риск развития аллергических реакций.
Постоянное использование специально разработанных для базового ухода за атопической кожей препаратов, способных эффективно восстанавливать нарушенный кожный барьер, помогает существенно снизить количество обострений и улучшить качество жизни больных с АД.
Следует отметить, что увлажняющие смягчающие средства не обладают противовоспалительным действием и в меньшей степени облегчают симптомы, определяющие тяжесть течения АД. Со своей стороны, противовоспалительные препараты не предназначены для лечения сухости кожи.
Топические противовоспалительные препараты
ТГКС — хорошо изученная группа лекарственных средств. Несмотря на появление нового класса противовоспалительных средств — ТИК, они остаются препаратами первой линии в лечении обострений заболевания.
Как известно, при бронхиальной астме алгоритм применения ингаляционных кортикостероидов разработан и предусматривает регулярное их использование в качестве поддерживающей терапии больным всех степеней тяжести заболевания. При АД подход к назначению ТГКС иной и связан прежде всего с высоким потенциальным риском развития местных нежелательных реакций. При назначении ТГКС следует учитывать тяжесть заболевания, место локализации и возраст больного.
В педиатрической практике широко используют синтетическое производное гидрокортизона — гидрокортизона-17-бутират (Локоид). Эстерификация гидрокортизона боковым звеном масляной кислоты по С17 позволила улучшить абсорбцию препарата через кожу и усилить его метаболизм. В результате гидрокортизона-17-бутират приобрел уникальное соотношение эффективность/безопасность: препарат относится к сильным стероидам (как бетаметазон 17-валерат или триамцинолон), но его местная и системная безопасности сравнимы с таким слабым стероидом, как гидрокортизон.
Препарат может применяться длительно (до 4 недель), разрешен к применению у детей начиная с 6-месячного возраста.
Отсутствие значимого угнетения гипоталамо-гипофизарно-надпочечниковой системы (ГГНС) при использовании гидрокортизона 17-бутирата у здоровых добровольцев и пациентов с АД подтверждено в ряде клинических исследований [7, 8].
Тормозящее влияние экзогенных кортикостероидов на гипофиз-адреналовую функцию вполне ожидаемо. Вместе с тем, как было недавно показано в оригинальном исследовании Haeck I. с соавторами, низкое содержание кортизола у больных с тяжелым течением АД в большей степени может быть связано со степенью тяжести самого заболевания, чем с применением ТГКС [9]. Авторы сравнивали базальный уровень кортизола в крови у 25 больных с тяжелой формой АД (1-я группа), которым требовалась госпитализация, и 28 амбулаторных больных со средней и тяжелой степенью тяжести АД (группа 2): у 80% пациентов 1-й группы уровень кортизола был достоверно ниже уровня больных 2-й группы (p
Д. Ш. Мачарадзе, доктор медицинских наук, профессор
РУДН, Москва
Себорейный дерматит
Замечено, что активность этих условно-патогенных грибов возрастает при неблагоприятных условиях, таких как:
Неблагоприятными факторами для усиления патологического процесса считаются:
Симптомы себорейного дерматита
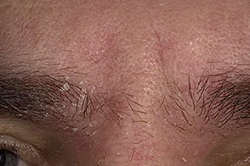
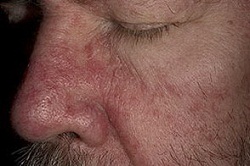
При себорейном дерматите поражение кожи носит постепенный, медленно прогрессирующий характер и сопровождается зудом, нередко, интенсивным. На себорейных участках на фоне пятен красного цвета появляются бляшки с довольно чёткими границами, образованные в результате слияния мелких узелков желтовато-розового цвета, покрытых жирными чешуйками. Процесс поражения кожи часто носит симметричный характер и за счёт периферического роста и разрешения в центре бляшки могут приобретать гирляндоподобные и кольцевидные формы.
На фото симптомы себорейного дерматита лица
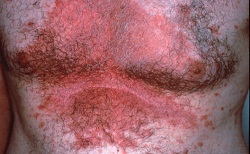
Патологический процесс, расположенный в складках (заушные, под молочными железами, в паху), часто сопровождается мокнутием, появлением липких корок и трещин.
На фото симптомы себорейного дерматита (носощёчные складки)
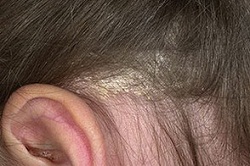
При поражении кожи волосистой части головы отмечается неравномерное шелушение или образование плотных корочек. Нередко при осмотре можно увидеть жёлтые или белые чешуйки, прикреплённые к стержню волоса, а также перхоть. Волосы при этом обычно истончаются и редеют, что в конечном итоге приводит к диффузной алопеции (облысению).
На фото симптомы себорейного дерматита волосистой части головы
На фото симптомы себорейного дерматита тела: эритродермия
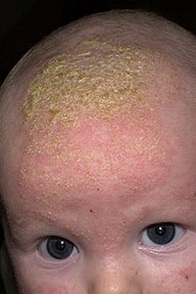
На фото симптомы себорейного дерматита у ребенка: молочный струп
Диагностика
При постановке диагноза себорейный дерматит необходимо исключать такие заболевания кожи как атопический дерматит, экзематид, псориаз, грибковые заболевания (стригущий лишай) и микробные поражения кожи. Для этого необходимо провести микроскопическое и микологическое исследование чешуек кожи на патогенные грибы. Иногда прибегают к диагностической биопсии, при которой в совокупности многочисленных признаков будут зафиксированы клетки-нейтрофилы в составе корок и чешуек, а также в устьях волосяных фолликулов. При себорейном дерматите, протекающем торпидно, необходимо дополнительное исследование гормонального статуса пациента.
Лечение
Известно, что на сегодняшний день не существует препаратов, нормализующих работу сальных желез, поэтому проблема лечения себорейного дерматита должна быть направлена на коррекцию проявлений отдельных симптомов.
1. Медикаментозная терапия – направлена на нормализацию обмена веществ.
Это, как правило, лечение основного заболевания: органов желудочно-кишечного тракта, заболеваний печени, поджелудочной железы, щитовидной железы.
Также назначаются витамины группы В, липоевая кислота, фолиевая кислота.
2. Наружняя терапия.
При локализации процесса на волосистой части головы в первую очередь отдается предпочтение специфическому противогрибковому лечению. При этом применяются шампуни, содержащие такие противогрибковые компоненты, как кетоконазол или циклопирокс, а также пиритион цинка и деготь. В лечении себорейного дерматита также используют другие шампуни с пиритионом цинка. Шампунь, содержащий одновременно и кетоконазол и цинк–пиритион, нередко помогает быстрее решить проблему себорейного дерматита волосистой части головы и вызвать более продолжительную ремиссию.
В последнее время всё активнее в дерматологии используются наружные иммуномодуляторы, обладающие также и противовоспалительной, и противогрибковой активностью. Это крема «Элидел» и «Протопик», которые могут использоваться на определённом этапе лечения себорейного дерматита, под контролем врача.
При поражении себорейным дерматитом кожи груди и спины используются все выше перечисленные средства. Это и шампуни, пена которых при мытье наносится на туловище, и противогрибковые крема, и болтушки и иммуномодуляторы для наружного применения.
3. Физиотерапия: местная физиотерапия и системная.
Применяется для снятия воспалительного процесса, для улучшения местного иммунитета и нормализации функции сальных желез.
Подбор местных физиотерапевтических методик осуществляется индивидуально, исходя из пола, возраста человека, остроты периода и характера себорейного дерматита.
Из системной физиотерапии активно используется внутривенное лазерное облучение крови, внутривенная озонотерапия.
Нужно отметить, что использование физиотерапии в лечении себорейного дерматита увеличивает скорость лечения, скорость восстановления тканей и стойкость эффекта лечения.