можно ли вылечить генитальный герпес навсегда
Генитальный герпес. Симптомы и лечение.
Пузырьки в интимной зоне
Как передается герпес
Вирус простого герпеса первого типа. Передать эту разновидность вируса можно воздушно-капельным путем при кашле, чихании, питье из чашки и тд. Чаще всего ВПГ 1 провоцирует высыпания на лице: поражение слизистых оболочек рта и носа, но может также протекать и бессимптомно или поражать область гениталий. Однако, избавится от этого вируса навсегда, увы, уже не получится. Вирус при лечении не погибает, а прячется в нервных ганглиях. Поэтому стоит только носителю вируса испытать сильный стресс или переохладится, как заболевание снова начнет прогрессировать.
Вирус простого герпеса второго типа. В отличие от первого типа, пузырьковая сыпь чаще появляется не на лице заболевшего, а на половых органах и зоне ануса. Передается ВПГ-2 чаще всего во время незащищенного полового контакта. К слову, презерватив не всегда может обеспечить 100% защиты от полового герпеса, так как жидкость из папул может остаться на бедрах и паховой зоне. ВПГ 2 также не исчезает из организма, а “живет” в нервных ганглиях на протяжении всей жизни заболевшего.
Герпес симптомы
Врачебное сообщество выделяет следующие варианты течения болезни.
После вскрытия пузырьков, на их месте появляются ярко-красные язвочки, которые заживают на протяжении недели-двух.
Рецидив
Фактор риска при беременности
Если женщина была носителем ВПГ до того, как забеременела, то ее иммунная система может защитить малыша, но в случае обострений сохраняется риск развития осложнений. Заражение ребенка возможно во время родов, при условии, что они пройдут во время активной фазы течения болезни. Поэтому важно пристально следить за своим здоровьем во время вынашивания малыша, чтобы не допустить рецидивов.
Лечение генитального герпеса
Как говорилось выше, способа полностью избавится от вируса простого герпеса невозможно, как и вылечить генитальный герпес навсегда. Однако современная медицина способна предложить лучшие средства от герпесаспособы, которые могут сдерживать возбудителя генитального герпеса в неактивном состоянии и значительно снизить вероятность возвращения симптомов как у мужчин, так и у женщин.
В таком случае лечение преследует три цели: избавить пациента от болезненной пузырьковой сыпи, зуда, предотвратить рецидив. В обязательном порядке назначаются противовирусные средства на основе ацикловира внутрь, а для уменьшения отека, зуда и воспаления назначаются средства местного действия. Одним из таких средств является спрей Эпиген Интим, который обладает противовирусным, иммуностимулирующим, противовоспалительным, противозудным и регенерирующим действием. Он усиливает действие основного противовирусного препарата, способствует выработке собственных интерферонов в очаге активности вируса, что может способствовать сокращению длительности острой фазы заболевания. Применение спрея Эпиген Интим также способствует устранению воспаления и зуда, ускорению заживления язвочек.
Профилактика генитального герпеса
Препарат может применяться не только в острую фазу заболевания, но и для профилактики возможных обострений, в том числе у беременных, когда противопоказано большинство противовирусных препаратов. В связи с невозможностью исцеления от генитального герпеса раз и навсегда, лучше заранее позаботиться о профилактике инфицирования ВПГ:
Также носитель вируса должен предупредить своего партнера об этом, даже если в настоящий момент ремиссия, ведь инфицирование возможно и в спокойный период.
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
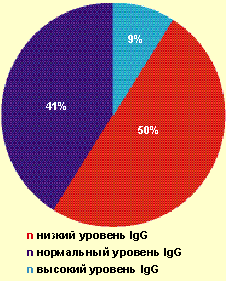 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
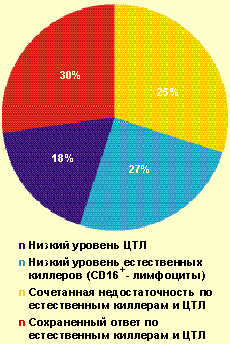 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва
Генитальный герпес: клинические вопросы, требующие однозначных ответов. Марченко Л.А.
Лариса Андреевна Марченко, профессор:
– Мы сегодня поговорим о генитальном герпесе, об использовании современных препаратов, которые появились на нашем рынке при такой патологии, как генитальная герпетическая инфекция. Я буду высказывать и свое мнение, и, безусловно, я буду опираться на документы, которые на сегодняшний день являются основополагающими. Это Европейские рекомендации по лечению генитальной герпетической инфекции, которые пролонгированы до мая 2013 года, и, к сожалению, срок пролонгации истек, но новых рекомендаций нет. И почему мы в большей степени опираемся на эти рекомендации? Потому что наш друг, Радж Пател, который два раза был в России, он возглавляет эти рекомендации. И приятно сказать, что профессор Гомберг Михаил Александрович, друг нашей клиники и друг всех акушеров-гинекологов России, он от России выступает экспертом, также и создателем этих рекомендаций, и поэтому на сегодняшний день мы работаем по этим рекомендациям.
Прежде всего, должна сказать, что 2013 год был таким эпохальным, потому что 100 лет с открытия вируса герпеса, и вирусологи хорошо изучили морфологию, антигенные структуры, механизмы репликации, все вирусологические свойства. А мы с вами клиницисты, и нам надо лечить, уметь лечить больных, страдающих генитальным герпесом. И вот до фактически 1974 года хорошо работал тезис о том, что количество лекарственных средств, используемых при генитальной герпетической инфекции, было обратно пропорционально их эффективности. И только в 1974 году создается аналог нуклеозидов ацикловир, и где-то через 10 лет Гертруда Элайон получает Нобелевскую премию за создание этого противовирусного препарата. Сами понимаете, вирус герпеса – это вирус, который поражает не только эпителиальную клетку, но и нервную клетку, и создавали препараты, и дали Нобелевскую премию, потому что от герпетических менингитов и энцефалитов смертность составляла более 80%. Тем не менее, получив Нобелевскую премию за создание этого препарата, фирмы не остановились, и в связи с тем, что все-таки биодоступность препарата была достаточно низкая относительно, 15-30%, также сродство с тимидинкиназой было не очень высокое, также относительно недолго находился препарат в клетке, возникали привыкания к препарату, и появились ацикловир-резистентные штаммы.
Через 10 лет появляется валиловый эфир ацикловира, и проходит еще 10 лет, и в 1994 году создается фамцикловир, последний препарат из этой группы, производная пенцикловира. И исследователям удается достичь уже 77%-ной биодоступности. Препарат долго находится в хорошей связываемости тимидинкиназой, до 20 часов находится в клетке, и практически привыкания к этому препарату пока еще не появилось. Но инфекция серьезная, генитальным герпесом на сегодняшний день, известно, страдает каждая пятая женщина нашей планеты в возрасте после 12 лет. Драматическая ситуация в Африке. А во всех развитых странах, включая Россию, примерно одинаковые показатели. 20% женщин в России страдает генитальной герпетической инфекцией. И особенности эпидемиологии, ключевая позиция при этой патологии заключается в том, что каждая пятая пациентка страдает генитальным герпесом, но вы как клиницист помните об очень маленьком количестве больных, у которых эта инфекция, перед вашими глазами, из 20 пациенток, которые теоретически страдают генитальным герпесом, перед глазами вот эти 4 красных человечка, у которых типичная форма герпеса с классической лихорадкой, которая повторяется в зависимости от того, 1-м или 2-м типом герпеса страдает женщина, ежемесячно или раз в год.
Вы совершенно не знаете о четырех женщинах, которые страдают бессимптомным проявлением герпеса, но у которых, к сожалению, в 70% случаев при бессимптомной форме погибнут дети от внутриутробной герпетической инфекции, и мать постфактум пойдет обследоваться на генитальную герпетическую инфекцию, потому что морфологи дадут заключение о том, что плод был инфицирован герпесом. И остальные пациентки из 20, здесь у нас 12, они будут страдать атипичной формой герпеса, которые будут приходить к врачу с жалобами на зуд, жжение, неприятные ощущения, бели. А вы если не обследуете их на наличие вируса герпеса, ДНК вируса герпеса в половом тракте, будете находиться в неведении, и не будете знать, как лечить этих пациенток. Но, к сожалению, долгое время считалось, что генитальным герпесом заболевают женщины, которые инфицированы 2 м типом вируса. Но на сегодняшний день уже почти каждая пятая и там третья больная инфицирована и 1-м типом, чего не было буквально 20 лет назад, потому что широко развиты орогенитальные контакты.
И вот мы, исследуя пациенток наших в Covance лаборатории в Швейцарии, показали, что в структуре инфицирования генитальным герпесом каждая третья больная инфицирована 1-м типом. Да, конечно, 50% – 2-м типом, и надо, конечно, с самого начала типировать пациенток, типировать обязательно, потому что известно – если клиника тяжелая, обострения каждый месяц, 6 и более обострений в год, а есть пациентки, которые 12 обострений имеют в год, уже заранее известно, что это 2-й тип герпеса, и не надо проводить им терапию эпизодически, лечить каждое обострение, а все-таки надо переходить к терапии супрессивной по отношению к возбудителю этой инфекции, и проводить длительные 6-8-месячные курсы лечения, дабы получить положительный эффект и не дискредитировать препараты, которые входят в линейку препаратов, которые получили Нобелевскую премию. Очень редко в нашей специальности дают за препараты Нобелевскую премию. Поэтому возникает вопрос: а вообще надо ли обязательно типировать, если классическая лихорадка герпетическая? Может быть, можно по внешнему виду поставить диагноз? Анкетирование достаточно большой группы женщин и мужчин показало, что на основе клинических симптомов трудно достаточно бывает заподозрить диагноз, а диагноз ставился с помощью типоспецифических антител, в России таких антител нет, когда по крови можно поставить диагноз.
Но по анамнезу достаточно по тому, как рассказывает нам пациентка, дебют заболевания, клинические проявления, достаточно трудно поставить диагноз, и все-таки надо, конечно, обязательно каждый случай подозрительный на генитальный герпес, а генитальный герпес – это венерическое заболевание, передаваемое половым путем, это трагедия большая для нашей пациентки, мы должны понимать, что и внутрисемейные отношения могут меняться. И если женщина или мужчина еще не в браке, у них какие-то ограничения в половых контактах. Конечно, мы должны поставить им четко диагноз, что это генитальный герпес, тем более, что есть заболевания, которые похожи, также сопровождаются язвенными проявлениями и похожи на герпес, но это не герпес. Чтобы не спутать герпес с сифилисом и с красным плоским лишаем, и с болезнью Бехчета (это очень интересное заболевание, но нет времени говорить), с рецидивирующим кандидозом. Кстати, у больных с генитальным герпесом в 30% случаев это причина рецидивирующей кандидозной инфекции. Поэтому если у больной 4 и более обострения кандиды в течение жизни, надо обследовать обязательно на генитальный герпес. Надо также проводить дифф. диагноз и с чесоткой, и с банальной травмой, и с пузырчаткой. Я, кстати, один раз не поставила, не знаю, дерматовенерологам иногда приходится показывать этих пациенток, потому что мы не сталкиваемся с пузырчаткой. И со стрептококковым импетиго, который, в общем, хорошо знают дерматологи, поэтому иногда приходится обращаться к нашим коллегам.
Поэтому на сегодняшний день методом диагностики является, конечно, четкий метод. Надо найти ДНК вируса герпеса 1-го или 2-го типа методом ПЦР в реальном времени. С высокой и специфичностью, и чувствительностью этот метод, он ничем не уступает классическому культуральному методу. Но, если вы в своих клиниках иммуноферментным методом, иммунофлуоресцентным методом пользуетесь, то от таких методов надо уходить, потому что они имеют очень низкую специфичность. Хочу сразу сказать, что вот бактериальные инфекции, когда мы правильно делаем онкоцитологию больным или, грамотней сказать, ПАП-тест, то параллельно мы определяем, какое количество лейкоцитов в мазке, какой тип клеток, то в рекомендациях четко записано: метод ПАП-теста не может ни в коем случае использоваться для постановки диагноза генитального герпеса, потому что в мазке вы ничего не увидите. Это надо помнить. Вот на сегодняшний день в России мы определяем, к сожалению, смешанные антитела в крови и к 1-му, и ко 2-му типу. И 95% нашего населения – носители 1-го и 2-го типа герпеса, комбинации этих типов. Поэтому по крови ставить диагноз генитального герпеса нельзя, потому что страдает 20%, а вы невольно цифру увеличите до 95%.
С помощью смешанных антител мы выявляем только группу больных, особенно беременных, когда мы смотрим на TORCH-инфекции, которые серонегативные по генитальной герпетической инфекции… – по инфекции герпетической, простите, не генитальной, а просто по герпетической инфекции в целом, – и потом в процессе беременности мы наблюдаем, не появилась ли сероконверсия к возбудителю просто герпесвирусной инфекции, и следим именно за 5% женщин, которые не имеют антител к герпесу. Поэтому ставить диагноз с помощью тестов по крови на сегодняшний день нельзя ни у нас в России, ни в мире, потому что вот эти типоспецифические антитела IgG2, они очень дорогие, и для клинической практики ими не пользуются на Западе. К ним прибегают на Западе, у нас их нет, потому что очень дорого стоят, только в случаях таких, которые трудноразрешимые в России, когда вы раз за разом видите герпетические высыпания, классическую герпетическую лихорадку, берете мазок из цервикального канала, и не находите возбудителя, не находите ДНК вирусную. Вот в этом случае прибегают к серологическим исследованиям.
Возникает вопрос: может быть, заражение, если вирус генитального герпеса можно исключить с помощью, если серонегативный анализ на антитела, и тоже это неправильно. По антителам – это дополнительный метод. В России очень любят ориентироваться на антитела. Нельзя, потому что они теоретически должны формироваться к 22-му дню от момента заражения, но у 20% они не формируются в течение ближайших 3 месяцев. Вот поэтому-то женщина, которая в первом триместре беременности серонегативная, ей надо брать во втором и в третьем триместре, следить за появлением серонегативности. Вот еще есть очень важный момент. Почему так много стало генитальной герпетической инфекции? Люди никто не хотят заражать друг друга в остром периоде, когда максимум высыпаний на половых органах. Но никто, к сожалению, не знает, что 7 дней до высыпания и 7 дней после того, как высыпания эти зажили, идет жесткая репродукция вируса, выделение вируса из предполагаемого очага, и в этот момент наши больные остаются источниками заражения.
Как можно снизить риск передачи инфекции? Конечно, использование презервативов, безусловно. Конечно, в первый год заболевания, понятно, наиболее высокий процент заражения в половой паре. Конечно, во время обострений, безусловно, нельзя жить половой жизнью. Но есть еще метод, который позволяет спокойно жить людям, которые находятся в дискордантных парах, то есть если один половой партнер страдает генитальным герпесом, а второй либо бессимптомный носитель, но он думает, что он здоров, или на самом деле здоров. Если пациентка страдающая, кстати, женщина, частыми тяжелыми формами генитального герпеса, она должна использовать фамцикловир в режиме супрессивной терапии, и у нее в 95% случаев она не будет выделять вирус, и риск передачи инфекции снижается на 48%. Это сделаны были международные исследования такие на примере валацикловира, но всего на 48%. Но это большое значение имеет, конечно. Осложнения, дает ли генитальный герпес? Я говорю сейчас о генитальном герпесе. Осложнения? Да, к сожалению. Особенно при первичном эпизоде, во время беременности. Также бывает, асептические менингиты, чаще они характерны для женщин, в три раза реже они встречаются у мужчин. Могут спорадические энцефалиты бывать.
Может развиться синдром Элсберга. Это синдром, который характеризует радикулоневропатиями, когда больная даже не может помочиться, у нее временная парализация нижних конечностей, сильные боли радикулярные. К счастью, они проходят на терапии аналогами нуклеозидов, и обязательно к этому лечению должны быть привлечены и специалисты невропатологи, в частности. Очень частый синдром Белла, когда неврит лицевого нерва при генитальном герпесе встречается. Значительно реже – поражения внутренних органов, могут быть даже гепатозы, пневмониты. И следует помнить, во всех случаях, когда есть обострения, обязательно надо начинать со специфической терапии аналогами нуклеозидов обязательно, и использовать обязательно, лечение должно проводиться совместно, обязательно привлекать специалистов невропатологов, дерматологов и так далее. Что касается того, как же мы должны интерпретировать наши результаты лабораторные, и как должны лечить наших пациенток. На сегодняшний день в мире существует жесткий один подход – использовать при генитальной герпетической инфекции аналоги нуклеозидов. К сожалению, Россия – особая страна, где пользуются либо иммуномодулирующей терапией, – возможно, иммуномодулирующая терапия это будущее в лечении генитального герпеса, но пока иммуномодуляторы не найдены, – либо комбинированной терапией. Но, с точки зрения фармакотерапии это вообще абсурд.
Если эффективность аналогов нуклеозидов 95%, зачем же увеличивать до 98, может быть, используя, добавляя иммуномодуляторы? Это нереально. Поэтому все-таки мы должны придерживаться рекомендаций международных, где написано, что генитальный герпес надо лечить аналогами нуклеозидов. И вот сегодня мы обсуждаем фамвир, препарат, производный от пенцикловира, и механизм действия препарата заключается в том, за это и была дана Нобелевская премия, что этот препарат, если у больной в организме нет острой репродукции вируса, а когда начинается репродукция вируса, выделяется фермент тимидинкиназы, который вообще ни в каких ситуациях в человеческом организме, кроме как острое инфицирование генитальным герпесом или экстрагенитальным герпесом, не появляется. Поэтому под влиянием тимидинкиназы фамцикловир из неактивной формы начинает превращаться в моно-, и трифосфат, и уже трифосфат обладает активным действием. Но хочу сразу вам сказать, что фамцикловир, согласно рекомендации FDA, равно как и валацикловир, не разрешен беременным. Поэтому мы сегодня беременности касаться не будем, и будем обсуждать лечение пациенток наших фамцикловиром вне беременности.
И еще раз подчеркиваю, почему сегодня мы говорим об этом препарате, – потому что препарат имеет высокую биодоступность, хорошее сродство с тимидинкиназой, и не формируется мутантных штаммов. Потому что у меня огромный опыт использования препаратов, и ацикловира, и валацикловира, и в ряде случаев больные получают препараты и говорят, что эффекта нет. У нас теперь есть новый препарат, который нам поможет в этих ситуациях. Невольно мы сами формируем мутантные штаммы, и в рекомендациях международных записано, что генитальный герпес – это болезнь всего организма, и поэтому сегодня уже никто не пользуется при этой патологии кремом ацикловира, потому что он ответственен как раз, считается, за развитие мутантных штаммов. Какие же режимы использования фамцикловира? При остром эпизоде, при первичном эпизоде генитального герпеса мы пользуемся фамцикловиром по 250 миллиграмм 3 раза в день не менее 5-7 дней, поэтому препарат существует в двух дозах – 250 миллиграмм и 125 миллиграмм. Причем, начинаем лечить препаратом сразу по подозрению.
Если диагноз генитального герпеса мы выставляем больной, получив положительный ответ ДНК-зонда, наличие генитального герпеса, то лечение начинаем сразу, как приходит к нам больная, и мы подозреваем только эту патологию. Потому что, если у нее нет генитального герпеса, если у нее эта язва обусловлена травмой, то тимидинкиназы не будет в организме, и препарат не окажет никакое действие, и неактивированный фамцикловир никак не воздействует на незараженные клетки, никакого отрицательного действия на организм не будет, а положительное будет, если мы рано начинаем лечить. Вот как раз на слайде показано, что, к сожалению, и вы должны это понимать, ни один аналог нуклеозидов на сегодняшний день не может вылечить больную от генитального герпеса, потому что в течение ближайших 48-72 часов вирус попадает в ганглии нервные, и там находится на протяжении 64 лет в виде голой ДНК. Потом, как только воздействует какой-то провоцирующий фактор, для женщин это часто менструация, поэтому обострение, инфицирование 2-м типом часто бывает связано с менструальными днями, вирус опять идет восходящим путем к тому месту, куда впервые попал. Но, если больная в супрессивном режиме получает препарат, он у нее находится все время в организме, она еще не знает, что у нее началось обострение, а выделенная тимидинкиназа активирует препарат, и идет как бы скрытое лечение.
Поэтому режим супрессивной терапии при тяжелых формах герпеса проводить необходимо. Но если у больной уже не первичный эпизод, а повторное обострение, то дозу можно в два раза уменьшить, и она составляет 125 миллиграмм, и уже не 3 раза в день, а 2 раза в день 5 дней. Кому дают такие режимы? Нашим пациенткам, у которых бывает мало обострений, в год бывает 1 обострение, 2 обострения. Если же 6 и более обострений в год, то такой режим ничего не дает. При таких ярких обострениях можно обострение резко укоротить, если в течение суток выпить одномоментно 4, по 4 таблетки 2 раза в день препарат, то прямо можно даже и это обострение в каждом четвертом случае оно будет очень быстро купироваться в течение нескольких даже часов. Если наша пациентка, как я вам сказала, страдает частыми обострениями, 6 и более обострений в год, это тяжелая форма герпеса, мы даем фамцикловир по 250 миллиграмм 2 раза в день. И как долго? До 12 месяцев. После этого надо сделать перерыв и посмотреть, какой режим обострений у пациентки будет. И вы скажете: «Что же это за препарат, который 12 месяцев мы должны давать нашим пациентам? Что же будет у них с печенью, с почками и так далее?» Ничего не будет. Потому что в течение 12 месяцев, на самом деле, обострение, может быть, препарат работает, может быть 20 дней, потому что он понимает, что произошла сборка вируса, появилась тимидинкиназа, в течение нескольких часов репродукция блокируется вируса, и опять препарат просто как по подозрению находится в организме, не оказывая никакого патологического воздействия на неинфицированные органы и системы.
Итак, эффективность фамцикловира высокая, 90%, и поэтому нам думается, что нет смысла изменять те режимы использования препаратов, которые на сегодняшний день предлагают Международные рекомендации, в частности, Европейские. Еще раз подчеркну, создателем этих рекомендаций являются наши отечественные профессора, в частности, дерматовенерологи. И вот такой красивый слайд. Вот так Сальвадор Дали представлял себе генитальный герпес. А на самом деле он совсем имеет другое обличие. Но фантазия, возможно, важнее знаний, говорил Эйнштейн. И, может быть, на этой основе мы создадим новые препараты. Благодарю за внимание.