что лучше фарингосепт или антиангин
Анти-ангин формула таблетки : инструкция по применению
Инструкция
Состав на одну таблетку
Вспомогательные вещества: левоментол, сахарин, сорбитол, кремния диоксид коллоидный безводный, магния стеарат, ароматизатор «анисовый», ароматизатор «мятный», краситель азорубин (Е-122).
Описание
Таблетки плоские, со скошенным краем, от бледно-розового до красновато-розового цвета с более светлыми и более тёмными вкраплениями, со специфическим запахом. На обеих сторонах таблетки гравировка «NP» на фоне дерева.
Фармакотерапевтическая группа
Прочие антисептические средства, применяемые при заболеваниях горла.
Антибактериальное действие хлоргексидина осуществляется за счет неспецифического связывания с фосфолипидами бактериальных клеточных мембран. Хлоргексидин может оказывать бактерицидное и бактериостатическое действие, преимущественно, в отношении грамположительных бактерий и Candida albicans, и в меньшей мере, против грамотрицательных бактерий. Хлоргексидин особенно активен в отношении Streptococcus mutans, Streptococcus salivarius, Escherichia coli, Selenomonas spp. и анаэробных бактерий. Препарат значительно менее эффективен в отношении таких видов микроорганизмов как Streptococcus sanguis, Proteus, Pseudomonas, Klebsiella veillonella.
Анестетик тетракаин оказывает местнообезболивающее действие.
Аскорбиновая кислота участвует в регуляции окислительно-восстановительных процессов, свертываемости крови, регенерации тканей, иммунных реакций.
Хлоргексидин практически не абсорбируется через слизистую оболочку и кожу. При рассасывании хлоргексидин постепенно высвобождается из таблеток в слюну и связывается со слизистой оболочкой ротовой полости и языка, после чего снова попадает в слюну, где проявляется его антибактериальное действие. Хлоргексидин проглатывают со слюной, однако его абсорбция из желудочно-кишечного тракта очень низкая. Хлоргексидин в незначительной степени метаболизируется в печени и выводится с желчью через кишечник. Обычно 90% попавшего в ЖКТ хлоргексидина выводится в неизмененном виде с калом.
Аскорбиновая кислота хорошо абсорбируется из желудочно-кишечного тракта. Степень ее связывания с белками плазмы крови составляет около 25%. Аскорбиновая кислота метаболизируется до дигидроаскорбиновой и щавелевой кислот, выводится с мочой.
Тетракаин, как большинство местных анестетиков, плохо абсорбируется через слизистые оболочки. Гидролизуется эстеразами в плазме и в меньшей степени в печени. Связывание с белками крови незначительное.
Показания к применению
Лечение инфекционно-воспалительных заболеваний полости рта и глотки (стоматит, гингивит, тонзиллит, фарингит, пародонтоз).
Клинически доказанная эффективность антисептического средства Фарингосепт (амбазон) за многолетний период его применения в медицинской практике
О.В. Кладова, д. м. н., профессор, кафедра инфекционных болезней у детей №1 педиатрического факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова МЗ РФ, г. Москва.
О.В. Шамшева, д.м.н., профессор, зав. кафедрой инфекционных болезней у детей №2 педиатрического факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова МЗ РФ, г. Москва.
Ключевые слова: антисептик, боль в горле, дети, амбазон, Фарингосепт®
Key words: antiseptic, sore throat, children, ambazone, Faringosept®
В конце 50-х и начале 60-х гг. XIX в. исследования Пастера выяснили значение микробов в процессах гниения белковых веществ. Английский хирург Листер, ознакомившись с открытием Пастера, в 1867 г. представил свои результаты по применению химических веществ при лечении ран. Работами Пастера и Листера было положено начало антисептике, получившей возможность вести борьбу с инфекцией.
На сегодняшний день насчитывается 2000 антибиотиков, в практике же активно используется около 50. Но с 1950 г. отмечены первые случаи устойчивости флоры к антибиотикам. Сегодня тенденции применения антибиотиков при респираторных заболеваниях в мире носят разноречивый характер, однако общим направлением является то, что практически у каждой страны разработан план надзора за необходимостью и целесообразностью применения антибиотиков при лечении данной патологии. Это в первую очередь связано с возрастающей резистентностью этих препаратов к бактериальной флоре. Так, по данным многоцентровых исследований, проведенных в начале нового столетия в нашей стране, в том или ином проценте случаев имеет место резистентность клинических штаммов. Значимую разницу в развитии резистентности представляют нозокомиальные штаммы, в частности S.aureus, который устойчив к эритромицину, тетрациклину до 50%, но не имеет устойчивости к линкозамидам, гликопеп-тидам, что еще раз может свидетельствовать о том, что при тяжелых формах заболевания эмпирическое назначение антибиотиков должно быть связано с препаратами из групп линко-замидов, гликопептидов, нитроимидазола, ами-ногликозидов и цефалоспоринов III-IV поколений, способных разрушить бактериальную пленку и воздействовать на патоген.
В настоящий момент при выборе медикаментозных средств большое значение отводится степени эффективности того или иного рекомендуемого препарата и профилю безопасности. Сегодня у прогрессивных врачей совершенно иные взгляды, отличающиеся от ранее принятых в схемах лечения. Врачи стараются меньше использовать препараты системного действия и больше уделять внимания местному лечению.
Одним из наиболее изученных антисептических препаратов является амбазон, разработанный Г. Домагком (Doinagk G) и С. Пе-терсеном (Petersen S) в 1955 г., который используется в клинической практике уже более 50 лет. Исследования, проведенные в период 1950-1960 гг., показали, что амбазон имеет антибактериальные топические свойства при введении в орофарингеальную полость и что он эффективен против патогенов, которые обычно вызывают инфекции на этом уровне (Streptococcus haemoliticus, Streptococcus viridans, Pneumococcusи т. д.). Амбазон имеет бак-териостатическое действие на гемолитические стрептококки при концентрациях в диапазоне от 1:1 000 000 до 1:10 000 000 (Lorenz K., 1960; Doinagk K., 1955; Suss K.-J. & Kettwig W., 1962). Амбазон проявляет умеренную эффективность в действии против стафилококка. Амбазон не вызывает никаких признаков дис-бактериоза в желудочно-кишечном тракте.
Как основное действующее вещество амбазон вошел в состав препарата Фарингосепт («Ранбакси») в 80-х гг. ХХ в., в России препарат зарегистрирован с 1986 г., то есть успешно применяется уже более 25 лет. За эти годы в России не выявлено ни одного серьезного побочного действия. Почему? Да потому, что действующее вещество амбазон является одним из самых безопасных местных антисептиков. Кроме того, в состав препарата входит сахароза, моногидрат лактозы, какао, ванилин или лимонный ароматизатор. У Фарингосепта нет побочных эффектов и противопоказаний (кроме индивидуальной непереносимости), он не вступает во взаимодействие с другими препаратами, не имеет негативного влияния на кишечную микрофлору. Учитывая тот факт, что Фарингосепт был одним из первых асептических препаратов для сублинг-вального применения на нашем рынке, на сегодняшний день он может восприниматься некоторыми специалистами как несовременный.
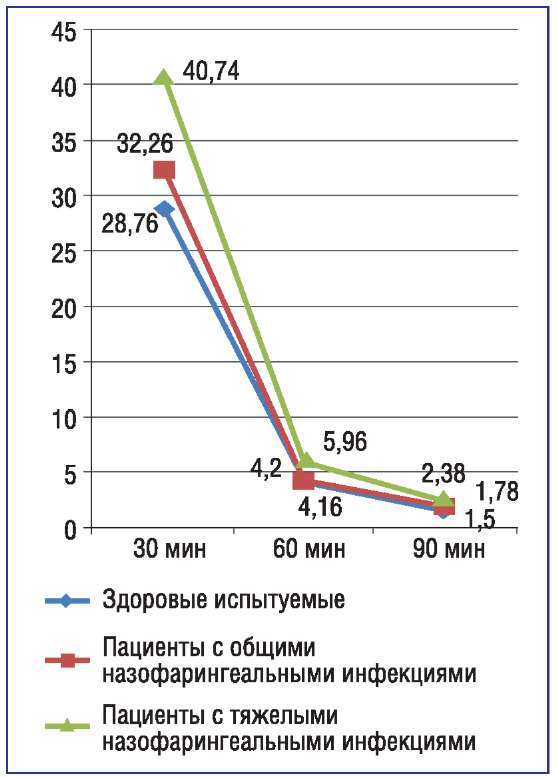
Рисунок. Концентрация амбазона (Фарингосепта) в слюне у больных с назофарингеальными инфекциями и здоровых пациентов через 30-60-90 минут после применения препарата
В состав Фарингосепта входит натуральный порошок какао, который известен не только приятным вкусом, но и успокаивающим и смягчающим действием, устраняет сухость, неприятные ощущения (першение, зуд и т. д.) и боль в горле. Следует напомнить, что в какао есть флавонои-ды, имеющие свойства антиоксидантов, защищающие организм от воздействия свободных радикалов, а также стимулирующие деятельность системы кровообращения.
Препарат, безусловно, нравится маленьким пациентам, так как для детей важен вкус препарата, а у Фарингосепта он «шоколадный». Препарат разрешен к применению лишь детям с 3 лет. Скорее всего, это связано с тем, что таблетки надо рассасывать. А совсем маленькие пациенты будут их просто разжевывать и глотать, при этом выраженного клинического эффекта можно не получить.
В настоящее время некоторые пациенты предпочитают лечить боль в горле «народными средствами», но большинство пациентов готовы сочетать «бабушкины рецепты» и современные препараты. Поэтому пациентам следует напомнить, что в Фарингосепте роль асептика выполняет амбазон, эффективность которого систематически оценивает фирма-производитель, и она нисколько не уменьшилась за 50-летний период его применения в медицинской практике.
Выпускается Фарингосепт в виде таблеток для рассасывания. Достаточно всего лишь положить таблетку в рот и рассосать ее до полного растворения, что приведет к быстрому бактерицидному и противовоспалительному действию.
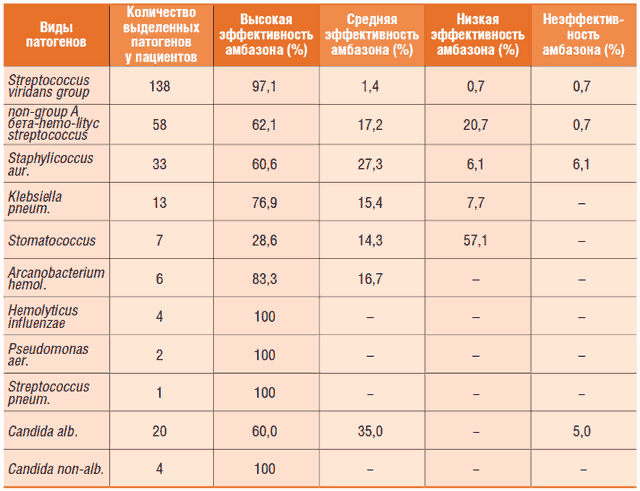
Таблица. Эффективность действия амбазона на патогенную микрофлору
Ученые из нескольких стран СНГ проводили исследования по эффективности применения Фарингосепта в лечении детей с заболеваниями горла. При этом сравнивались старые методы с использованием препаратов общего действия, местного лечения в виде полоскания горла растворами антисептиков и Фарингосепта. Оказалось, что при применении Фарингосепта клиническое улучшение наступило раньше, а побочных эффектов при этом у пациентов не наблюдалось вообще. Фарингосепт совершенно не влияет на микробиологическое равновесие в кишечнике пациента, сколько бы таблеток в день пациент ни принял. Еще один плюс препарата Фарингосепт заключается в том, что он обладает высоким профилем безопасности, не имеет противопоказания «беременность». Не выявлено никаких взаимодействий с иными лекарственными препаратами, поэтому прием Фарингосепта можно сочетать с любыми другими местными и системными препаратами.
Таблетки для рассасывания очень удобны в использовании, в том числе на работе или в поездке. Фарингосепт сочетает в себе высокую эффективность, подтвержденную специалистами в клинических исследованиях, и приемлемую цену для любого пациента. Так, упаковки № 20 и № 10 доступны для всех потребителей и обеспечивают как курсовое, так и спорадическое применение.
Список литературы находится в редакции.
Лечение острого и хронического фарингита
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Отделение оториноларингологии Центральной клинической больницы Медицинского центра Управления делами Президента РФ
Ф арингитом называют острое или хроническое воспаление слизистой оболочки глотки, которое сопровождается болями, першением или дискомфортом в горле. Поскольку с анатомической точки зрения глотка делится на три отдела – верхний (носоглотка), средний (ротоглотка) и нижний (гортаноглотка), воспалительные процессы, развивающиеся здесь, можно также подразделить в соответствии с их преимущественной локализацией. Однако деление это будет весьма условным, особенно при остром фарингите, из–за того, что острые вирусные и бактериальные инфекции диффузно поражают слизистую оболочку верхних дыхательных путей и носят мигрирующий, чаще нисходящий характер. Морфологические изменения слизистой оболочки при хроническом фарингите обычно имеют преимущественную локализацию в одном из анатомических отделов глотки, что позволяет с долей условности выделять отдельные нозологии, например, хронический назофарингит.
Этиология и классификация
По этиологическому фактору острые фарингиты можно разделить на вирусные, бактериальные, грибковые, аллергические, травматические (следствие попадания инородного тела или хирургического вмешательства) и вызванные воздействием раздражающих факторов (горячей жидкости или пара, кислот, щелочей, облучения и др.). Хронические фарингиты обычно классифицируют не по этиологическому признаку, а по характеру развивающихся в слизистой оболочке изменений: катаральный (простой), атрофический (субатрофический) и гипертрофический. Указанные формы хронического воспаления часто сочетаются. Так, наличие диффузных атрофических изменений в слизистой оболочке может сочетаться с очаговой гиперплазией лимфоидной ткани задней стенки глотки или тубофарингеальных валиков.